Bài 10 (trang 245 SGK Hóa 11 nâng cao)
Đề bài
Bài 10 (trang 245 sgk Hóa 11 nâng cao): oxi hóa 4,6 gam hỗn hợp chứa cùng số mol của hai ancol đơn chức, thành anđêhit thì dùng hết 7,95 gam CuO. Cho toàn bộ lượng anđêhit thu được tác dụng với dung dịch AgNO3 trong NH3 thì thu được 32,4 gam Ag. Xác định công thức cấu tạo hai ancol đó. Biết các phản ứng xảy ra hoàn toàn.
Hướng dẫn giải
Thiết nghĩ đề bài nên cho khối lượng CuO là 8 gam, không càn cho giả thiết “có cùng số mol” và đề bài nên báo rõ ràng là quá trình oxi hóa tạo ra hai anđêhit (ancol chỉ biến thành anđehit) để bài toán giải nhẹ nhàng hơn, phù hợp với suy nghĩ của các em học sinh hơn.
Số mol CuO là : 8/80=0,1 (mol); số mol Ag: 32,4/108=0,3 (mol)
Về nguyên tắc bài tập này phải xet qua hai trường hợp sau đây:
Trường hợp 1: hai ancol đơn chức bậc 1 ⇒ hai anđehit đơn chức
Hai anđêhit đơn chức tráng gương lại phải xét tiếp hai trường hợp nhỏ
Trường hợp a: hai anđêhit là HCHO và RCHO (R ≠ 1)
Trường hợp b: hai anđêhit là RCHO và R'CHO(R,R' ≠ 1)
Trường hợp 2: một ancol đợn chức bậc một ⇒ một anđêhit đơn chức.
Một anđêhit tráng gương lại phải xét tiếp hai trường hợp nhỏ
Trường hợp a: anđêhit là HCHO
Trường hợp b: anđêhit là RCHO (R khác 1)
Tuy nhiên ancol tác dụng với CuO theo tỉ lệ mol 1: 1 , anđêhit đơn chức tráng gương với tỉ lệ mol 1; 2 chỉ có ancol bậc một và bậc hai mới bị oxi hóa bởi CuO.
Như vậy, ta có nNaOH ≤ nCuO = 0,1 mol⇒nAg ≤ 0,2 mol. Nhưng ở đây nAg = 0,3 mol ⇒ hỗn hợp đầu là hai ancol đơn chức bậc một và có một ancol là CH3 OH (x mol).
Đặt công thức tổng quát của ancol thứ hia là RCH2 OH (y mol)
Sơ đồ hợp thức của quá trình oxi hóa và tráng gương
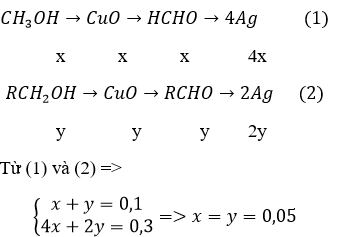
khối lượng hỗn hợp ancol ⇒ 0,05.32 + 0,05(R + 31) = 4,6 ⇒ R = 29 (C2H5)
vậy công thức cấu tạo của hai ancol là: CH3 OH và CH3 CH2 CH2 OH

