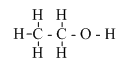Tổng hợp lý thuyết chính xác nhất về rượu etylic
Bài viết được Cunghocvui tổng hợp về những kiến thức về ancol etylic như công thức rượu etylic, tính chất hóa học của rượu etylic, ứng dụng của rượu etylic, cách điều chế rượu etylic, mối liên hệ giữa etilen rượu etylic và axit axetic, công thức tính độ rượu etylic . Mong rằng sau bài viết các bạn có thể nhận biết rượu etylic axit axetic và chất béo, hay nhận biết rượu etylic axit axetic và glucozo, và chỉ ra được khối lượng riêng của rượu etylic.

I) Rượu etylic
1) Công thức cấu tạo phân tử
Rút gọn: \(CH_3 - CH_2 - OH\)
- Gốc -OH làm cho rượu có tính chất hóa học đặc trưng.
2) Độ rượu và công thức tính độ rượu etylic
- Là số mililit rượu etylic nguyên chất có trong 100ml hỗn hợp rượu etylic với nước
- Công thức tính: Độ rượu = \(\dfrac {V_{C_2H_5OH nguyenchat}}{V_{dd}(C_2H_5OH + H_2O)}.100\)
Trong đó: V được đo bằng mililit hoặc lít
II) Tính chất vật lí và tính chất hóa học của rượu etylic
1) Tính chất vật lí
- Chất lỏng không màu
- Nhiệt độ sôi: \(78,3^0C\)
- Nhẹ hơn nước nhưng tan vô hạn trong nước
- Hòa tan được nhiều chất: iot, benzen,...
2) Tính chất hóa học
a) Phản ứng cháy
Rượu etylic cháy với ngọn lửa màu xanh, tỏa nhiều nhiệt trong quá trình phản ứng
VD: \(2C_2H_5 + 2Na \rightarrow 2CO_2 + 3H_2O\)
b) Phản ứng với kim loại
- Cho một mẩu natri vào cốc đã đựng rượu etylic, khi phản ứng mẩu natri tan dần và có bọt khí thoát ra.
\(2C_2H_5 + 2Na \rightarrow 2C_2H_5ONa + H_2\)
c) Phản ứng với axit axetic
- Đun nóng hỗn hợp một thời gian thì xuất hiện chất lỏng không màu, mùi thơm, không tan trong nước (nổi trên mặt nước)
VD: \(C_2H_5OH + CH_3COOH \rightleftharpoons CH_3COOC_2H_5 + H_2O\) (xúc tác là axit sunfuric đặc)
III) Ứng dụng - Điều chế
1) Những ứng dụng của rượu etylic
- Trong công nghiệp: làm nhiên liệu cho động cơ ô tô, cho đèn cồn trong phòng thí nghiệm
- Là nguyên liệu sản xuất axit axetic, dược phẩm, cao su tổng hợp
- Pha chế các loại rượu uống
2) Cách điều chế rượu etylic
a) Cách 1
Điều chế để làm đồ uống: \(C_6H_{12}O_6 \overset{men ruou}{\rightarrow} 2CO_2 + 2C_2H_5OH\)
b) Cách 2
Sản xuất phụ vụ ngành công nghiệp: \(CH_2 = CH_2 + H_2O \overset{axit}{\rightarrow} C_2H_5OH\)
♦Lưu ý: Một số chất có công thức phân tử chung là \(C_nH_{2n+1}OH\) (ancol no, đơn chức, ankanol) có tính chất tương tự rượu etylic.
Có thể bạn quan tâm: Lý thuyết về axit axetic chính xác nhất
IV) Mở rộng sơ đồ mối liên hệ giữa etilen rượu etylic và axit axetic
\(Etilen \xrightarrow[axit]{+nuoc}\) Rượu etylic \(\xrightarrow[mengiam]{+oxi}\) Axit axetic \(\xrightarrow[H_2SO_4đ, t^o]{+C_2H_5OH}\) Etyl Axetat
V) Luyện tập
Bài 1: Hãy dựa vào những bài đã học ở phía trước rồi đưa ra cách nhận biết rượu etylic axit axetic và chất béo và cách nhận biết rượu etylic axit axetic và glucozo.
Bài 2: Tính m(g) axit axetic thu được sau khi lên men 50 lít rượu etylic 4 độ. Biết rằng khối lượng riêng của rượu etylic là 0,8g/ml và hiệu suất quá trình lên men là 92%.
Trên đây là bài viết mà Cunghocvui đã tổng hợp được về tính chất vật lí và tính chất hóa học của rượu etylic, mối liên hệ giữa etilen rượu etylic và axit axetic, công thức rượu etylic, ứng dụng của rượu etylic, cách điều chế rượu etylic và công thức tính độ rượu etylic.