Phản ứng este hóa và bài tập hiệu suất phản ứng este hóa
Phản ứng este hóa và bài tập hiệu suất phản ứng este hóa
Phản ứng este hóa là một dạng bài hết sức cơ bản và thường xuất hiện trong đề thi. Tuy nhiên, nó lại gây không ít khó khăn cho học sinh trong quá trình tìm hiểu phương pháp giải. Nhận thấy được điều đó, chúng tôi đã soạn lên bài giảng này với hy vọng giúp đỡ được các bạn trong học tập!
I. Lý thuyết chung
Phản ứng este hóa là gì?
Phản ứng este hóa là điều chế este bằng phản ứng giữa rượu đơn chức hoặc đa chức với axit hữu cơ đơn chức hoặc đa chức
Ví dụ: phản ứng este hóa giữa ancol etylic và axit axetic.
| C2H5OH | + | CH3COOH | ⇌ | H2O | + | CH3COOC2H5 | |
| lỏng | lỏng | lỏng | lỏng | ||||
| không màu | không màu | không màu |
Đặc điểm của phản ứng este hóa là phản ứng thuận nghịch
II. Hiệu suất phản ứng este hóa
1. Công thức
Cách 1: Tính theo lượng chất ban đầu cần lấy
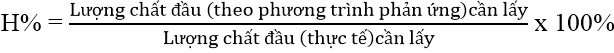
Cách 2: Tính theo lượng sản phẩm phản ứng thu được:
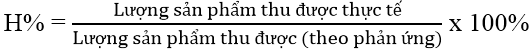
Ví dụ:
Bài 1: 9,2g C3H5(OH)3 với 60g Ch3COOH. Giả sử chỉ thu được C3H5(OOCCH3) với lượng 17,44g. Áp dụng công thức tính hiệu suất của phản ứng xảy ra:
Hướng dẫn:
n C3H5(OH)3 = 0,1 mol
n CH3COOH = 1 mol
Ta có phản ứng xảy ra:
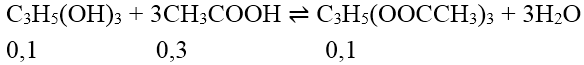
Cân bằng phương trình trên ta có đẳng thức:
\(m_{este}\) = 0,1.218 = 21,8g
Tuy nhiện theo giá trị thực tại: \(m_{este}\) = 17,44g
Áp dụng công thức ta có hiệu suất cần tìm là: \(H\% = \dfrac{17,44}{21,8}.100 = 80\%\)
Tham khảo: Phản ứng este hóa
2. Bài tập phản ứng este hóa
Trên đây là toàn bộ kiến thức chúng tôi muốn chia sẻ về phản ứng este hóa, cùng học vui chúc các bạn đạt được điểm số cao!

