Lý thuyết căn bản liên kết cộng hóa trị dễ nhớ nhất
Cùng với Cunghocvui đi vào tìm hiểu các kiến thức về liên kết cộng hóa trị lớp 10. Bài viết sẽ đưa ra cho bạn cách viết liên kết cộng hóa trị, phân biệt liên kết ion và liên kết cộng hóa trị, liên hệ tới bài giảng liên kết ion và sau cùng sẽ là tổng hợp bài tập liên kết ion và liên kết cộng hóa trị.
I) Liên kết cộng hóa trị
1) Định nghĩa
- Liên kết được tạo nên từ hai nguyên tử bằng một hoặc nhiều cặp e chung thì gọi là liên kết cộng hóa trị.
2) Phân loại
Có 2 loại là liên kết cộng hóa trị không phân cực và phân cực.
a) Liên kết cộng hóa trị không phân cực
- Liên kết trong các phân tử tạo nên từ 2 nguyên tử của cùng 1 nguyên tố có độ âm điện như nhau, nên cặp e dùng chung không bị lệch về phía nguyên tử nào thì được gọi là liên kết cộng hóa trị không phân cực.
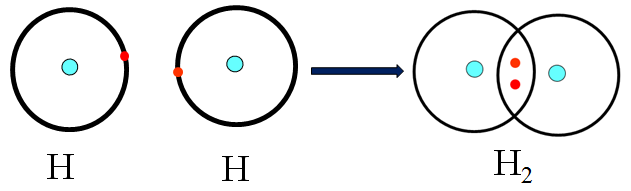
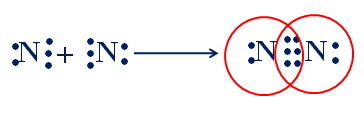
- Trong liên kết cộng hóa trị không phân cực thì lại có hai loại: liên kết là liên kết đơn ( ở phân tử \(H_2\)) và liên kết ba ( ở phân tử \(N_2\))
b) Liên kết cộng hóa trị phân cực
- Liên kết cộng hóa trị mà trong đó cặp e chung bị lệch về phía nguyên tử có độ âm điện lớn hơn thì gọi là liên kết cộng hóa trị phân cực.
- Cặp e chung được đặt về phía kí hiệu của nguyên tử có độ âm điện lớn hơn.
II) Các bước cách viết công thức cộng hóa trị
- B1: Xác định cấu hình e của các nguyên tử.
- B2: Xác định số e còn thiếu để đạt cấu hình bền của khí hiếm, sao cho số e góp chung bằng số e thiếu.
- B3: Viết công thức e thỏa mã quy tắc bát tử.
♦ Quy tắc bát tử:
- Khái niệm: Là quy tắc viết công thức e của nguyên tử sao cho đảm bảo số e đạt cấu hình bền của khí hiếm bằng 8.
- Quy tắc đúng với những nguyên tố thuộc chu kì I và II bởi từ chu kì 3 trở đi đã có phân lớp d, tạo nhiều liên kết hơn, xung quanh nguyên tử có nhiều hơn 8.
III) Cách phân biệt liên kết ion và liên kết cộng hóa trị

(Bảng phân biệt liên kết ion và liên kết cộng hóa trị không cực và liên kết cộng trị có cực)
Có thể bạn quan tâm: bài giảng liên kết ion
IV) Tổng hợp bài tập liên kết ion và liên kết cộng hóa trị
Bài 1: So sánh sự giống và khác nhau của liên kết cộng hóa trị và liên kết ion.
Bài 2: Hãy giải thích sự hình thành liên kết ion, lấy ví dụ cụ thể cho việc giải thích.
Bài 3: Có một bạn học sinh phát biểu như sau: "Liên kết cộng hóa trị có cực được tạo thành giữa 2 nguyên tử có hiệu độ âm điện từ 0,4 đến nhỏ hơn 1,7". Theo bạn phát biểu này đúng hay sai?
Bài 4: Thế nào là liên kết ion, liên kết cộng hóa trị không phân cực, liên kết cộng hóa trị phân cực? Lấy ví dụ minh họa cụ thể.
Bài 5: Cho các chất: \(AlCl_3, CaCl_2, Cá, Al_2S_3\). Hãy dựa hiệu độ âm điện các nguyên tố ở bảng 6 trang 45 SGK và cho biết rằng có loại liên kết nào trong các chất trên?
Xem thêm >>> Hướng dẫn bài tập SGK
Trên đây là bài viết mà Cunghocvui đã tổng hợp về liên kết cộng hóa trị lớp 10, hy vọng sau bài viết này bạn có thể phân biệt liên kết hóa ion và liên kết cộng hóa trị, biết được cách biết liên kết cộng hóa trị và thành thạo bài tập liên kết ion và liên kết cộng hóa trị. Chúc bạn học tập tốt <3