216 Bài tập tổng hợp Hóa vô cơ cực hay có lời giải...
- Câu 1 : Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
A. thạch cao nung
B. đá vôi.
C. boxit
D. thạch cao sống
- Câu 2 : Cho các nhóm tác nhân hoá học sau:
A. (1), (3), (4).
B. (2), (3), (4).
C. (1), (2), (4).
D. (1), (2), (3).
- Câu 3 : Tiến hành thí nghiệm với các dung dich muối clorua riêng biệt của các cation: X2+, Y3+, Z3+, T2+. Kết quả được ghi ở bảng sau:
A. Ba2+, Fe3+, Al3+, Cu2+
B. Ca2+, Au3+, Al3+, Zn2+.
C. Ba2+, Cr2+, Fe3+, Mg2+
D. Mg2+, Fe3+, Cr3+, Cu2+
- Câu 4 : Cho mẫu nước cứng chứa các ion: Ca2+, Mg2+ và . Hoá chất không thể dùng để làm mềm mẫu nước cứng trên là
A. K3PO4
B. Na2CO3
C. Ca(OH)2
D. HCl
- Câu 5 : Dãy gồm các ion (không kể sự điện li của H2O) cùng tồn tại trong một dung dịch là
A. Cu2+, NO3–, H+, Cl–.
B. Fe2+, K+, OH–, Cl–.
C. Ba2+, HSO4–, K+, NO3–.
D. Al3+, Na+, S2–, NO3–.
- Câu 6 : Cho dãy chuyển hóa sau: X Y + Z ; Y Z + CO2 + H2O
A. NaHCO3
B. (NH4)2CO3
C. Na2CO3
D. NH4HCO3
- Câu 7 : Cho dãy biến đổi sau: Cr X Y Z T
A. CrCl2, CrCl3, NaCrO2, Na2CrO4
B. CrCl2, CrCl3, NaCrO2, Na2Cr2O7
C. CrCl2, CrCl3, NaCrO2, Na2CrO7
D. CrCl2, CrCl3, Cr(OH)3, Na2CrO4
- Câu 8 : Kết luận nào sau đây không đúng ?
A. Thuốc thử đặc trưng dể nhận biết ion NO3– trong dung dịch muối nitrat là Cu
B. Thuốc thử đặc trưng để nhận biết ion Cl– là dung dịch AgNO3/HNO3.
C. Thuốc thử đặc trưng dể nhận biết anion SO42– là dung dịch BaCl2/HNO3
D. Thuốc thử có thể dùng để nhận biết HCO3–, CO32– là axit mạnh
- Câu 9 : Hấp thụ hoàn toàn 4,48 lít CO2 (đktc) vào 200 ml dung dịch chứa Na2CO3 0,5M và NaOH 0,75M thu được dung dịch X. Cho BaCl2 dư vào X, khối lượng kết tủa thu được là
A. 15,76 gam
B. 19,70 gam
C. 9,85 gam
D. 7,88 gam
- Câu 10 : Trong các mệnh đề sau, mệnh đề nào không đúng ?
A. SO2 và NOx gây mưa axit.
B. CO2 và CH4 gây hiệu ứng nhà kính.
C. Các ion kim loại nặng, các anion , thuốc bảo vệ thực vật và phân bón hóa học là tác nhân gây ô nhiễm môi trường nước.
D. Các chất ma túy thường gặp là: heroin, moocphin, cocain, amphetamin, nicotin.
- Câu 11 : Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ chất rắn X như sau:
A. NH4Cl NH3 ↑ + HCl ↑
B. CaC2 + 2H2O → Ca(OH)2 + C2H2
C. BaSO3 BaO + SO2 ↑
D. 2KMnO4 K2MnO4 + MnO2 + O2 ↑
- Câu 12 : Hỗn hợp X gồm Na, K, Na2O và K2O. Hòa tan hoàn toàn 25,7 gam X vào nước, thu được 3,36 lít khí H2 (đktc) và dung dịch Y, trong đó có 22,4 gam KOH. Hòa tan hết 0,4 mol H3PO4 vào Y, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 61,0
B. 77,2
C. 49,0
D. 64,0
- Câu 13 : Có 4 lọ dung dịch riêng biệt X, Y, Z và T chứa các chất khác nhau trong số bốn chất: (NH4)2CO3, KHCO3, NaNO3, NH4NO3. Bằng cách dùng dung dịch Ca(OH)2 cho lần lượt vào từng dung dịch, thu được kết quả sau
A. T là dung dịch (NH4)2CO3
B. Y là dung dịch KHCO3
C. Z là dung dịch NH4NO3.
D. X là dung dịch NaNO3.
- Câu 14 : Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Giá trị của m là
A. 50,87 gam.
B. 53,42 gam.
C. 55,34 gam.
D. 53,85 gam.
- Câu 15 : Cho m gam hỗn hợp gồm Na2O và Al2O3 vào 400 ml dung dịch H2SO4 0,3M và HCl 0,9M. Sau khi kết thúc phản ứng, thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X, phản ứng được biểu diễn theo đồ thị sau:
A. 9,84 gam.
B. 17,20 gam.
C. 16,04 gam.
D. 11,08 gam.
- Câu 16 : Trong số các nguồn năng lượng: (1) thuỷ điện, (2) gió, (3) mặt trời, (4) hoá thạch, những nguồn năng lượng sạch là
A. (1), (3), (4).
B. (2), (3), (4).
C. (1), (2), (4).
D. (1), (2), (3).
- Câu 17 : Phát biểu sai là:
A. Phương pháp trao đổi ion làm giảm tính cứng của nước cứng tạm thời và nước cứng vĩnh cửu
B. Thạch cao sống có công thức là CaSO4.H2O
C. Hàm lượng cacbon có trong gang cao hơn trong thép
D. Phèn chua có công thức KAl(SO4)2.12H2O được dùng làm trong nước đục
- Câu 18 : Phản ứng nào sau đây xảy ra ở điều kiện thường ?
A. 3C + 4CrO3 → 2Cr2O3 + 3CO2
B. C + H2O → CO + H2
C. C + CO2 → 2CO
D. C + 2H2 → CH4
- Câu 19 : Một học sinh làm thí nghiệm điều chế NH3 bằng cách đun nóng NH4Cl với Ca(OH)2, khí NH3 sinh ra thường có lẫn hơi nước. Vậy để làm khô khí NH3 cần dùng hóa chất nào sau đây?
A. NaCl (rắn)
B. dung dịch H2SO4 đặc
C. CuSO4 (rắn)
D. CaO (rắn)
- Câu 20 : Một mẫu K và Ba tác dụng với H2O dư thu được dung dịch X và 3,36 lít H2. Tính thể tích dung dịch H2SO4 2M cần dùng để trung hoà dung dịch X
A. 150 ml
B. 200 ml
C. 300 ml
D. 75 ml
- Câu 21 : Muốn tăng cường sức chống bệnh, chống rét và chịu hạn cho cây người ta dùng loại phân bón nào
A. Supephotphat
B. KCl
C. NH4Cl
D. Amophot
- Câu 22 : Phương trình hóa học sai là
A. 2Cr + 6HCl → 2CrCl3 + 3H2
B. Cu + 2FeCl3 → CuCl2 + 2FeCl2
C. Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
D. 3Mg (dư) + 2FeCl3 → 3MgCl2 + 2Fe
- Câu 23 : Tiến hành các thí nghiệm sau: (a) Cho Mg vào dung dịch Fe2(SO4)3 dư.
A. 4
B. 2
C. 3
D. 5
- Câu 24 : Dung dịch X chứa các ion: Ca2+, Na+, HCO3- và Cl–, trong đó số mol của ion Cl– là 0,07. Cho 1/2 dung dịch X phản ứng với dung dịch NaOH (dư), thu được 2 gam kết tủa. Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2 (dư), thu được 4,5 gam kết tủa. Mặt khác, nếu đun sôi đến cạn dung dịch X rồi nung đến khối lượng không đổi thì thu được m gam chất rắn. Giá trị của m là
A. 6,865.
B. 6,645
C. 8,79.
D. 8,625.
- Câu 25 : Cho các thí nghiệm sau (a) Cho dung dịch Ca(OH)2 dư vào dung dịch Ca(HCO3)2.
A. 3
B. 2
C. 4
D. 1
- Câu 26 : Cho các thí nghiệm sau: (a) Cho 1 mol NaHCO3 tác dụng với 1 mol KOH trong dung dịch.
A. 4
B. 6
C. 5
D. 3
- Câu 27 : Cho hỗn hợp gồm Na, K, Ba vào 200 ml dung dịch CuCl2 0,6M. Sau khi kết thúc các phản ứng, thu được 2,24 lít khí H2 (đktc) và m gam kết tủa. Giá trị m là
A. 4,90 gam.
B. 19,60 gam.
C. 9,80 gam.
D. 11,76 gam.
- Câu 28 : Phương án nào sau đây không đúng?
A. Cs được dùng làm tế bào quang điện.
B. Thạch cao sống được dùng để nặn tượng, đúc khuôn và bột bó khi gãy xương...
C. Na2CO3 là hóa chất quan trọng trong công nghiệp thủy tinh, bột giặt ...
D. Ca(OH)2 được dùng rộng rãi trong nhiều ngành công nghiệp: sản xuất amoniac, clorua vôi, vật liệu xây dựng...
- Câu 29 : Hòa tan hết m gam hỗn hợp Na, Na2O và ZnO vào 300 ml dung dịch NaOH 0,5M thu được dung dịch X và 1,792 lít khí H2 (đktc). Cho từ từ dung dịch HCl 1M vào X, đến khi bắt đầu xuất hiện kết tủa thì đã dùng 80 ml. Nếu cho 320 ml hoặc 480 ml dung dịch HCl 1M vào X, đều thu được a gam kết tủa. Giá trị của m là
A. 24,08 gam.
B. 23,60 gam.
C. 22,22 gam.
D. 19,43 gam.
- Câu 30 : Điện phân (điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi) V lít dung dịch X chứa đồng thời R(NO3)2 0,45M (R là kim loại hóa trị không đổi) và NaCl 0,4M trong thời gian t giây, thu được 6,72 lít hỗn hợp khí ở anot (đktc). Nếu thời gian điện phân là 2t giây thì thu được dung dịch Y. Dung dịch Y tác dụng vừa đủ với 400 ml dung dịch chứa KOH 0,75M và NaOH 0,5M, không sinh ra kết tủa. Biết hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của V là
A. 0,75
B. 2,00
C. 0,50
D. 1,00
- Câu 31 : Phương trình hóa học nào sau đây là sai ?
A. Fe + CuSO4 → FeSO4 + Cu
B. Cu + H2SO4 → CuSO4 + H2
C. 2Na + 2H2O → 2NaOH + H2
D. Ca + 2HCl → CaCl2 + H2.
- Câu 32 : Khí sinh ra trong trường hợp nào sau đây không gây ô nhiễm không khí?
A. Quá trình đốt nhiên liệu trong động cơ ô tô.
B. Quá trình đốt nhiên liệu trong lò cao
C. Quá trình quang hợp của cây xanh.
D. Quá trình đun nấu, đốt lò sưởi trong sinh hoạt.
- Câu 33 : Hiện tượng xảy ra khi nhỏ vài giọt dung dịch H2SO4 vào dung dịch Na2CrO4 là:
A. Dung dịch chuyển từ màu da cam sang màu vàng
B. Dung dịch chuyển từ màu vàng sang màu da cam
C. Dung dịch chuyển từ màu vàng sang không màu
D. Dung dịch chuyển từ không màu sang màu da cam
- Câu 34 : Từ hai :muối X và Y thực hiện các phản ứng sau
A. MgCO3, NaHCO3
B. CaCO3, NaHCO3
C. CaCO3, NaHSO4
D. BaCO3, Na2CO3
- Câu 35 : Thứ tự từ trái sang phải của một số cặp oxi hóa - khử trong dãy điện hóa như sau: Mg2+/Mg; Al3+/Al; Cr2+/Cr; Zn2+/Zn; Fe2+/Fe; Cu2+/Cu. Dãy chỉ gồm các kim loại tác dụng được với Zn2+ trong dung dịch là
A. Mg, Al, Zn
B. Al, Fe, Cu
C. Mg, Al, Cr
D. Cr, Fe, Cu
- Câu 36 : Thực hiện sơ đồ chuyển hóa sau (đúng với tỉ lệ mol các chất):
A. Đốt cháy 1 mol Y thu được Na2CO3 và 8 mol hỗn hợp gồm CO2, H2O, N2
B. Z tác dụng tối đa với CH3OH/HCl thu được sản phẩm có công thức C7H14O4NCl
C. Z có tính lưỡng tính
D. Dung dịch X làm quỳ tím hóa xanh
- Câu 37 : Trộn dung dịch X (NaOH 0,1M và Ba(OH)2 0,2M) với dung dịch Y (HCl 0,2M và H2SO4 0,1M) theo tỉ lệ nào về thể tích để được dung dịch có pH = 13
A 5:3
B. 4:5
C. 5:4
D. 3:2
- Câu 38 : Hấp thụ hết 4,48 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Lấy 100 ml dung dịch X cho từ từ vào 300 ml dung dịch HCl 0,5M thu được 2,688 lít khí (đktc). Mặt khác, 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 39,4 gam kết tủa. Giá trị của x là
A. 0,15
B. 0,1
C. 0,06
D. 0,2
- Câu 39 : Cho một lượng tinh thể Cu(NO3)2.3H2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A, đến khi khối lượng dung dịch giảm 18,65 gam thì dừng điện phân. Nhúng thanh Fe vào dung dịch sau điện phân, kết thúc phản ứng thu được 0,035 mol khí NO (sản phẩm khử duy nhất của N+5; đồng thời khối lượng thanh Fe giảm 2,94 gam. Thời gian điện phân là:
A. 6176 giây
B. 6948 giây
C. 8106 giây
D. 7334 giây
- Câu 40 : Phát biểu nào sau đây đúng ?
A. Nước cứng là nước chứa nhiều ion HCO3–, SO42–, Cl–.
B. Các kim loại kiềm thổ đều cùng kiểu mạng tinh thể lập phương tâm diện.
C. Hỗn hợp tecmit (dùng để hàn gắn đường ray) gồm bột Fe và Al2O3.
D. Thành phần chính của quặng boxit là Al2O3.2H2O.
- Câu 41 : Khi tiến hành thí nghiệm sinh ra các khí độc như SO2, H2S, Cl2, NO2. Để hạn chế các khí này thoát ra từ ống nghiệm một cách có hiệu quả nhất đồng thời tiết kiệm nhất, chúng ta thường nút ống nghiệm bằng bông tẩm dung dịch nào ?
A. Dung dịch nước vôi trong, Ca(OH)2.
B. Dung dịch Ba(OH)2.
C. Dung dịch xút ăn da, NaOH.
D. Dung dịch potat ăn da, KOH.
- Câu 42 : Hợp chất nào sau đây không tan trong dung dịch NaOH loãng dư ?
A. Cr2O3.
B. K2Cr2O7.
C. NaCrO2.
D. CrO3.
- Câu 43 : Nung m gam đá vôi có chứa 80% CaCO3 được V lít CO2 (đktc). Cho lượng CO2 thu được tác dụng với dung dịch có chứa 80 gam NaOH chỉ cho được một muối hiđrocacbonat X duy nhất. Giá trị của m là
A. 200.
B. 250.
C. 160.
D. 125.
- Câu 44 : Ba dung dịch X, Y, Z thoả mãn:
A. NaHCO3, NaHSO4, BaCl2.
B. Al2(SO4)3, BaCl2, Na2SO4.
C. FeCl2, Ba(OH)2, AgNO3.
D. NaHSO4, BaCl2, Na2CO3.
- Câu 45 : Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO2. Dẫn toàn bộ khí CO2 thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
A. 31,52.
B. 15,76.
C. 11,82.
D. 27,58.
- Câu 46 : Cho 61,25 gam tinh thể MSO4.5H2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, trong thời gian t giây, thấy khối lượng catot tăng m gam; đồng thời ở anot thu được 0,15 mol khí. Nếu thời gian điện phân là 2t giây, tổng số mol khí thoát ra 2 cực là 0,425 mol. Giá trị m là
A. 12,80 gam
B. 13,44 gam
C. 12,39 gam
D. 11,80 gam
- Câu 47 : Trường hợp nào sau đây không xảy ra phản ứng hóa học?
A. Cho Cr(OH)3 vào dung dịch NaOH loãng
B. Cho bột Fe vào dung dịch CrSO4
C. Cho dung dịch NaOH vào dung dịch K2Cr2O7
D. Cho dung dịch H2SO4 vào dung dịch Na2CrO4
- Câu 48 : Khí thải công nghiệp và của các động cơ ô tô, xe máy… là nguyên nhân chủ yếu gây ra mưa axit. Thành phần hóa học chủ yếu trong các khí thải trực tiếp gây ra mưa axit là:
A. CO, NO
B. CO, NO2
C. CO2, N2
D. SO2, NO2
- Câu 49 : Mẫu nước cứng chứa các ion: Mg2+, Ca2+, Cl‒, SO42‒ và HCO3‒. Nhận định sai là:
A. Mẫu nước trên làm mất tác dụng của xà phòng
B. Nếu dùng mẫu nước trên để nấu thức ăn sẽ làm thức ăn mau chín nhưng giảm mùi vị.
C. Mẫu nước trên có cả tính cứng tạm thời và tính cứng vĩnh cửu
D. Dùng dung dịch Na2CO3 có thể làm mềm tính cứng của mẫu nước cứng trên
- Câu 50 : Quan sát sơ đồ thí nghiệm sau:
A. Bản chất của quá trình điều chế là một phản ứng trao đổi ion
B. Do HNO3 có phân tử khối lớn hơn không khí nên mới thiết kế ống dẫn hướng xuống
C. Quá trình phản ứng là một quá trình thuận nghịch, trong đó chiều thuận là chiều toả nhiệt
D. HNO3 sinh ra trong bình cầu ở dạng hơi nên cần làm lạnh để ngưng tụ
- Câu 51 : Hấp thụ hết a mol khí CO2 vào dung dịch chứa NaOH 1M và Ba(OH)2 0,4M. Sau khi kết thúc các phản ứng, thu được 15,76 gam kết tủa và dung dịch X. Cho từ từ dung dịch HCl 1M vào X đến khi bắt đầu có khí thoát ra thì đã dùng 120 ml. Giá trị của a là
A. 0,12
B. 0,16.
C. 0,18.
D. 0,20
- Câu 52 : Cho hỗn hợp gồm Mg và Zn có tỉ lệ mol tương ứng 2 : 1 vào 500 ml dung dịch Fe2(SO4)30,2M và CuSO4 0,3M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y và m gam rắn Z. Cho dung dịch NaOH dư vào dung dịch Y, lấy kết tủa nung ngoài không khí đến khối lượng không đổi, thu được 15,2 gam hỗn hợp chứa 2 oxit. Giá trị của m là
A. 12,88 gam
B. 9,60 gam
C. 17,44 gam
D. 13,32 gam
- Câu 53 : Tiến hành điện phân dung dịch chứa m gam hỗn hợp CuSO4 và KCl bằng dòng điện một chiều có cường độ 2A (điện cực trơ, có màng ngăn xốp). Kết quả thí nghiệm được ghi trong bảng sau:
A. 14,70
B. 17,00
C. 18,60.
D. 16,30
- Câu 54 : Hòa tan hoàn toàn m gam hỗn hợp chất rắn X gồm Ba, BaO, Na, Al2O3 chỉ thu được dung dịch Y và 10,08 lít khí H2 (đktc). Nhỏ từ từ dung dịch H2SO4 vào dung dịch Y thu được kết quả như đồ thị dưới đây:
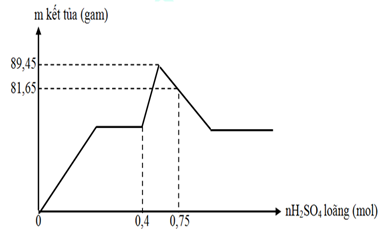
A. 78
B. 76
C. 73
D. 75
- Câu 55 : Hiện tượng xảy ra khi cho dung dịch KOH loãng vào dung dịch K2Cr2O7 là
A. Không có hiện tượng chuyển màu.
B. Dung dịch từ màu vàng chuyển sang màu da cam.
C. Xuất hiện kết tủa trắng.
D. Dung dịch từ màu da cam chuyển sang màu vàng.
- Câu 56 : Cho a gam hỗn hợp bột gồm Ni và Cu vào dung dịch AgNO3 (dư). Sau khi kết thúc phản ứng thu được 54 gam chất rắn. Mặt khác cũng cho a gam hỗn hợp 2 kim loại trên vào dung dịch CuSO4 (dư), sau khi kết thúc phản ứng thu được chất rắn có khối lượng (a + 0,5) gam. Giá trị của a là
A. 33,7 gam.
B. 53,5 gam.
C. 15,5 gam.
D. 42,5 gam.
- Câu 57 : Hòa tan 17 gam hỗn hợp X gồm K và Na vào nước được dung dịch Y và 6,72 lít H2 (đktc). Để trung hòa một nửa dung dịch Y cần dùng dung dịch hỗn hợp H2SO4 và HCl (tỉ lệ mol 1 : 2). Tổng khối lượng muối được tạo ra trong dung dịch sau phản ứng là
A. 21,025 gam.
B. 20,65 gam
C. 42,05 gam.
D. 14,97 gam.
- Câu 58 : Dung dịch X chứa Na2CO3 0,75M và NaHCO3 0,25M. Cho từ từ đến hết 200 ml dung dịch H2SO4 vào 200 ml dung dịch X thu được 3,36 lít khí (đktc) và dung dịch Y. Cho Ba(OH)2 dư vào dung dịch Y thu được m gam kết tủa. Giá trị m là
A. 56,45 gam
B. 54,65 gam
C. 44,80 gam
D. 34,95 gam
- Câu 59 : X, Y, Z là ba dung dịch không màu, thực hiện các thí nghiệm và có kết quả theo bảng sau:
A. NaHCO3, NaHSO4, BaCl2.
B. NaHSO4, BaCl2, Na2CO3.
C. Al2(SO4)3, BaCl2, Na2CO3.
D. FeCl2, Ba(OH)2, AgNO3.
- Câu 60 : Cho CO2 từ từ vào dung dịch hỗn hợp gồm Ca(OH)2 và KOH, ta có kết quả thí nghiệm được biểu diễn theo đồ thị dưới đây (số liệu tính theo đơn vị mol):
A. 0,12.
B. 0,13.
C. 0,11.
D. 0,10.
- Câu 61 : Nung hỗn hợp X gồm a gam Mg và 1,125 mol Cu(NO3)2, sau một thời gian, thu được chất rắn Y và 2,025 mol hỗn hợp khí Z gồm NO2 và O2. Cho Y phản ứng vừa đủ với dung dịch chứa 5,85 mol HCl, thu được dung dịch chỉ chứa m gam hỗn hợp muối clorua và 0,225 mol hỗn hợp khí T (gồm N2 và H2 có tỉ khối so với H2 là 11,4. Giá trị của (a + m) gần nhất là
A. 355,77.
B. 325,77.
C. 365,55.
D. 323,55.
- Câu 62 : Hòa tan hết 17,6 gam hỗn hợp X gồm Mg, MgCO3 và FeCO3 trong hỗn hợp dung dịch chứa 1,12 mol NaHSO4 và 0,16 mol HNO3. Sau khi kết thúc phản ứng, thấy thoát ra hỗn hợp khí Y gồm CO2, N2O và 0,08 mol H2; đồng thời thu được dung dịch Z chỉ chứa các muối sunfat trung hòa. Tỉ khối của Y so với He bằng 6,8. Cho dung dịch NaOH đến dư vào dung dịch Z, lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được 22,8 gam rắn khan. Phần trăm khối lượng của Mg đơn chất trong hỗn hợp X gần nhất với
A. 66,83%.
B. 64,12%.
C. 62,75%.
D. 65,35%.
- Câu 63 : Phát biểu không đúng là
A. Crom là kim loại màu trắng ánh bạc, cứng nhất trong các kim loại, có thể rạch được thủy tinh
B. Nhôm là nguyên tố phổ biến nhất trong vỏ trái đất
C. Trong tự nhiên, sắt chủ yếu tồn tại ở dạng hợp chất
D. Dung dịch K2Cr2O7 có màu da cam, dung dịch K2CrO4 có màu vàng
- Câu 64 : Một dung dịch X chứa 0,01 mol Ba2+, 0,01 mol NO3-, a mol OH-, b mol Na+. Để trung hòa 1/2 dung dịch X cần dùng 200 ml dung dịch HCl 0,1M. Khối lượng chất rắn thu được khi cô cạn dung dịch X là
A. 1,68 gam
B. 3,36 gam
C. 3,42 gam
D. 2,56 gam
- Câu 65 : Để làm khô, sạch khí NH3 có lẫn hơi nước người ta dùng
A. đặc
B. CaO
C. Na
D.
- Câu 66 : Đồ thị nào ứng với các thí nghiệm a, b, c:
A. a-1, b-2, c-3
B. a-2, b-3, c-1
C. a-3, b-1, c-2
D. a-3, b-2, c-1
- Câu 67 : Tiến hành thí nghiệm như hình vẽ, ban đầu trong cốc chứa dung dịch nước vôi trong, đóng khoá để dòng điện chạy trong mạch:
A. Mờ dần đi, rồi tắt hẳn
B. Ban đầu không đổi, sau đó sáng dần lên
C. Ban đầu mờ dần đi, sau đó vẫn mờ
D. Ban đầu mờ dần đi, sau đó sáng dần lên
- Câu 68 : Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch: CuSO4, NaOH, NaHSO4, K2CO3, Ca(OH)2, H2SO4, HNO3, MgCl2, HCl, Ca(NO3)2. Số trường hợp có phản ứng xảy ra là
A. 9
B. 7
C. 6
D. 8
- Câu 69 : Cho các phát biểu sau đây:
A. 4
B. 5
C. 2
D. 3
- Câu 70 : Dãy gồm các chất đều có thể làm mất tính cứng tạm thời của nước là
A. HCl, NaOH, Na2CO3
B. HCl, Ca(OH)2, Na2CO3
C. NaOH, Na3PO4, Na2CO3
D. KCl, Ca(OH)2, Na2CO3
- Câu 71 : Trong phòng thí nghiệm, khí amoniac được điều chế bằng cách cho muối amoni tác dụng với kiềm (ví dụ Ca(OH)2) và đun nóng nhẹ. Hình vẽ nào sau đây biểu diễn phương pháp thu khí NH3 tốt nhất ?
A. Hình 3
B. Hình 1
C. Hình 4
D. Hình 2
- Câu 72 : Phát biểu nào dưới đây sai ?
A. Phụ nữ sau sinh, hay bị choáng do thiếu máu nên bổ sung thêm nguyên tố canxi
B. Heroin và cần sa đều thuộc nhóm chất ma túy
C. Cafein, rượu đều thuộc nhóm chất gây nghiện
D. β-Caroten là tiền chất vitamin A giúp tránh khô mắt và giúp sáng mắt hơn
- Câu 73 : Hòa tan 5,73 gam hỗn hợp X gồm NaH2PO4, Na2HPO4 và Na3PO4 vào nước dư thu được dung dịch Y. Trung hòa hoàn toàn Y cần 75 ml dung dịch NaOH 1M, thu được dung dịch Z. Khối lượng kết tủa thu được khi cho Z tác dụng hết với dung dịch AgNO3 dư là
A. 16,776 gam.
B. 18,385 gam.
C. 18,855 gam.
D. 12,57 gam.
- Câu 74 : Thực hiện các thí nghiệm sau:
A. 5
B. 3
C. 4
D. 6
- Câu 75 : Dãy các ion nào sau đây có thể cùng tồn tại trong một dung dịch:
A. Fe2+, H+, Na+, Cl-, NO3-
B. Mg2+, HCO3-, SO42-, NH4+
C. Fe3+, Cl-, NH4+, SO42-, S2-
D. Al3+, K+, Br-, NO3-, CO32-
- Câu 76 : Cho các hợp kim sau: Cu-Fe (1); Zn-Fe (2); Fe-C (3); Sn-Fe (4); Fe-Cr-Ni (5). Để lâu các hợp kim trên trong không khí ẩm, số trường hợp xảy ra ăn mòn điện hóa là
A. 4
B. 5
C. 3
D. 2
- Câu 77 : Cho hai muối X, Y thoả mãn điều kiện sau:
A. Fe(NO3)3; NaHSO4
B. NaNO3 ; NaHSO4
C. NaNO3 ; NaHCO3
D. Mg(NO3)2 ; KNO3
- Câu 78 : Phát biểu nào sau đây là đúng ?
A. Photpho đỏ có khả năng phản ứng mạnh hơn photpho trắng
B. Thuỷ tinh lỏng là dung dịch đậm đặc của Na2SiO3 và K2SiO3
C. Cacbon monoxit và silic đioxit là oxit axit
D. Nitrophotka là hỗn hợp của NH4H2PO4 và KNO3
- Câu 79 : Thí nghiệm nào sau đây sau khi kết thúc phản ứng, thu được natri hiđroxit?
A. Cho dung dịch chứa 2a mol NaHCO3 vào dung dịch chứa a mol Ca(OH)2
B. Cho dung dịch chứa a mol NaHCO3 vào dung dịch chứa a mol Ca(OH)2
C. Cho Na2O vào dung dịch CuSO4 dư
D. Điện phân dung dịch NaCl bằng điện cực trơ, không màng ngăn xốp
- Câu 80 : Cho sơ đồ các phản ứng sau:
A. 5
B. 6
C. 4
D. 3
- Câu 81 : Tiến hành điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi. Kết quả quá trình điện phân được ghi theo bảng sau
A. Giá trị của V là 4,480 lít
B. Giá trị của m là 44,36 gam
C. Giá trị của V là 4,928 lít
D. Giá trị của m là 43,08 gam
- Câu 82 : Khẳng định sai là:
A. Cho CrO3 vào lượng dư dung dịch NaOH, thu được dung dịch có màu da cam
B. Kim loại đồng tan được trong dung dịch hỗn hợp NaNO3 và HCl
C. Tính chất vật lý chung của kim loại là tính dẻo, tính dẫn điện, dẫn nhiệt và tính ánh kim
D. Đun nóng mẫu nước cứng tạm thời thấy khí không màu thoát ra
- Câu 83 : Kết luận nào sau đây không đúng khi nói về 4 kim loại: Ca, Al, Fe và Cr
A. Fe và Cr tác dụng với dung dịch H2SO4 loãng theo cùng tỉ lệ mol
B. Cr là kim loại cứng nhất, có thể rạch được thủy tinh
C. Có 3 kim loại không thể tác dụng với dung dịch HNO3 đặc, nguội
D. Ca có nhiệt độ nóng chảy thấp nhất
- Câu 84 : Cho m gam dung dịch muối X vào m gam dung dịch muối Y, thu được 2m gam dung dịch Z chứa hai chất tan. Cho dung dịch BaCl2 dư hoặc dung dịch Ba(OH)2 dư vào Z, đều thu được a gam kết tủa. Muối X, Y lần lượt là:
A. NaHCO3 và NaHSO4.
B. Na2CO3 và NaHCO3.
C. Na2SO4 và NaHSO4.
D. NaOH và KHCO3.
- Câu 85 : Cho hỗn hợp rắn X gồm các chất có cùng số mol gồm BaO, NaHSO4, FeCO3 vào lượng nước dư. Lọc lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được chất rắn Y chứa :
A. BaSO4, BaO và Fe2O3.
B. BaSO4.
C. BaO và BaSO4.
D. BaSO4 và Fe2O3.
- Câu 86 : Cho dãy các chất: Ca(HCO3)2, NH4Cl, (NH4)2CO3, Al, Zn(OH)2, CrO3, Cr2O3. Số chất lưỡng tính trong dãy là
A. 5
B. 4
C. 3
D. 6
- Câu 87 : Khi sục từ từ CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
A. 4 : 5
B. 4 : 9
C. 9 : 4
D. 5 : 4
- Câu 88 : Cho các phát biểu sau:
A. 5
B. 4
C. 3
D. 2
- Câu 89 : Có 3 kim loại X, Y, Z thỏa mãn các tính chất sau:
A. Fe, Mg, Zn.
B. Zn, Mg, Al.
C. Fe, Al, Mg.
D. Fe, Mg, Al.
- Câu 90 : Nhận định nào sau đây là không đúng ?
A. Phân lân nung chảy là hỗn hợp muối photphat và silicat của canxi và magie, và chỉ phù hợp với đất chua.
B. Trong phòng thí nghiệm, để điều chế nhanh một lượng nhỏ NH3, ta cho NH4Cl tác dụng với Ca(OH)2.
C. Để thu được khí CO2 sạch và khô ta dẫn lần lượt hỗn hợp (CO2, HCl, H2O) qua dung dịch NaHCO3 và H2SO4 đặc.
D. Thứ tự lực axit giảm dần là: HNO3, H3PO4, H2CO3, H2SiO3.
- Câu 91 : Cho V1 ml dung dịch NaOH 0,4M vào V2 ml dung dịch H2SO4 0,6M. Sau khi kết thúc phản ứng thu được dung dịch chỉ chứa một chất tan duy nhất. Tỉ lệ V1 : V2 là
A. 1 : 3
B. 3 : 2
C. 3 : 1
D. 2 : 3
- Câu 92 : Xét các phát biểu:
A. 3
B. 1
C. 2
D. 4
- Câu 93 : Có 5 hỗn hợp, mỗi hỗn hợp gồm 2 chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu và Fe2(SO4)3; KHSO4 và KHCO3; BaCl2 và CuSO4; Fe(NO3)2 và AgNO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra các chất tan tốt trong nước là
A. 2
B. 4
C. 5
D. 3
- Câu 94 : Cho hỗn hợp X gồm Mg và Fe vào 200 ml dung dịch chứa Cu(NO3)2 1M và AgNO3 0,5M đến khi kết thúc các phản ứng được 24,16 gam hỗn hợp kim loại và dung dịch Y. Cho Y tác dụng với HCl dư được 0,224 lít NO (sản phẩm khử duy nhất, đktc). Phần trăm khối lượng của Fe trong hỗn hợp X có giá trị gần nhất với:
A. 28
B. 31
C. 30
D. 29
- Câu 95 : Rót từ từ dung dịch X chứa a mol Na2CO3 và 2a mol NaHCO3 vào dung dịch chứa 1,5a mol HCl thu được V lít khí CO2 (đktc) và dung dịch Y. Cho lượng khí CO2 ở trên từ từ cho đến hết vào dung dịch chứa b mol Ba(OH)2 ta có đồ thị sau:
A. 92,64.
B. 68,44
C. 82,88
D. 76,24
- Câu 96 : Cho hỗn hợp X gồm 0,24 mol FeO; 0,20 mol Mg và 0,10 mol Al2O3 tan hoàn toàn trong dung dịch chứa đồng thời 0,30 mol H2SO4 (loãng) và 1,10 mol HCl, thu được dung dịch Y và khí H2. Nhỏ từ từ dung dịch hỗn hợp Ba(OH)2 0,2M và NaOH 1,2M vào Y đến khi thu được khối lượng kết tủa lớn nhất, lọc kết tủa đem nung đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m gần nhất với:
A. 105,04.
B. 86,90.
C. 97,08.
D. 77,44.
- Câu 97 : Hình vẽ sau mô tả thí nghiệm điều chế khí Z ?
A. 2HCl + Zn → ZnCl2 + H2
B. K2Cr2O7 + 14HCl → 2KCl + 3Cl2 + 2CrCl3 + 7H2O
C. 4HNO3 đặc + Cu → 2NO2 + Cu(NO3)2 + 2H2O
D. Ca(OH)2 + 2NH4Cl rắn → 2NH3 + CaCl2 + 2H2O
- Câu 98 : Chất X được sử dụng trong quá trình sản xuất nhôm trong công nghiệp để giảm nhiệt đô nóng chảy của nhôm oxit, tăng khả năng dẫn điện của hỗn hợp nóng chảy... X là
A. Bôxit.
B. Đôlômit.
C. Manhetit.
D. Criolit.
- Câu 99 : Trong phòng thí nghiệm, người ta tiến hành thí nghiệm của kim loại Cu với dung dịch HNO3 đặc. Biện pháp xử lí tốt nhất để khí tạo thành khi thoát ra ngoài gây ô nhiễm môi trường ít nhất là
A. nút ống nghiệm bằng bông khô.
B. nút ống nghiệm bằng bông tẩm dung dịch Ca(OH)2.
C. nút ống nghiệm bằng bông tẩm nước.
D. nút ống nghiệm bằng bông tẩm cồn.
- Câu 100 : Tiến hành thí nghiệm như hình vẽ sau:
A. NH4Cl.
B. Na2CO3.
C. NaCl.
D. NH4NO2.
- Câu 101 : Thí nghiệm nào sau đây có phản ứng hóa học xảy ra
A. Cho Cr2O3 vào dung dịch NaOH loãng.
B. Cho bột Fe vào dung dịch HNO3 đặc, nguội.
C. Cho dung dịch Fe(NO3)3 vào dung dịch AgNO3.
D. Nhỏ dung dịch Br2 vào dung dịch chứa NaCrO2 và NaOH.
- Câu 102 : Có các dung dịch muối AlCl3, (NH4)2SO4, NH4NO3, MgCl2, FeCl3 đựng trong các lọ riêng biệt bị mất nhãn. Đánh dấu ngẫu nhiên 5 mẫu thử tương ứng với X, Y, Z, T, U rồi nhỏ từ từ dung dịch Ba(OH)2 vào các mẫu thử trên thì thu được kết quả trong bảng như sau:
A. FeCl3, (NH4)2SO4, NH4NO3, MgCl2, AlCl3.
B. FeCl3, NH4NO3, (NH4)2SO4, AlCl3, MgCl2.
C. FeCl3, NH4NO3, (NH4)2SO4, MgCl2, AlCl3.
D. FeCl3, (NH4)2SO4, NH4NO3, AlCl3, MgCl2.
- Câu 103 : Cho hỗn hợp rắn gồm Na2O, BaO, NaHCO3, Al2O3 và NH4Cl có cùng số mol vào nước dư. Kết thúc các phản ứng thu được dung dịch X. Dung dịch X chứa các chất tan là
A. BaCl2, NaAlO2, NaOH.
B. Na2CO3, NaCl và NaAlO2.
C. AlCl3, NaCl, BaCl2.
D. NaCl và NaAlO2.
- Câu 104 : Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100 ml dung dịch gồm K2CO3 0,2M và KOH x mol/lít, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y. Cho toàn bộ Y tác dụng với dung dịch BaCl2 (dư), thu được 11,82 gam kết tủa. Giá trị của x là
A. 1,4.
B. 1,2.
C. 1,6.
D. 1,0.
- Câu 105 : Tiến hành các thí nghiệm sau :
A. 4
B. 5
C. 6
D. 7
- Câu 106 : Điện phân dung dịch chứa m gam KCl có màng ngăn, điện cực trơ cho đến khi dung dịch chứa 2 chất tan có cùng nồng độ mol thì dừng lại thu được dung dịch X. Hấp thụ 0,2m gam CO2 vào dung dịch X thu được dung dịch Y chứa 37,0778 gam chất tan. Rót từ từ dung dịch chứa x mol HCl vào dung dịch Y thu được 0,896 lít CO2 (đktc). Giá trị của x là
A. 0,108.
B. 0,117.
C. 0,124.
D. 0,136.
- Câu 107 : Hỗn hợp X gồm a mol Mg và 2a mol Fe. Cho hỗn hợp X tác dụng với O2, sau một thời gian thu được (136a + 11,36) gam hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HNO3 dư thu được 3 sản phẩm khử có cùng số mol gồm NO, N2O, NH4NO3. Cô cạn dung dịch sau phản ứng thu được 647a gam chất rắn khan. Đốt hỗn hợp X bằng V lít hỗn hợp khí Cl2 và O2 (đktc) thu được hỗn hợp Z gồm các oxit và muối clorua (không còn khí dư). Hòa tan hỗn hợp Z cần vừa đủ 0,8 lít dung dịch HCl 2M, thu được dung dịch T. Cho dung dịch T tác dụng với dung dịch AgNO3 dư thu được 354,58 gam kết tủa. Giá trị của V là:
A. 15,68
B. 14,56
C. 16,80
D. 12,32
- Câu 108 : Điều khẳng định nào sau đây là sai?
A. Cho dung dịch HCl loãng, dư vào dung dịch alanin, thấy dung dịch phân lớp
B. Nhỏ dung dịch H2SO4 đặc vào saccarozơ sẽ hoá đen
C. Cho dung dịch glucozơ vào dung dịch AgNO3/NH3 đun nóng xuất hiện kết tủa trắng bạc
D. Cho dầu ăn vào ống nghiệm đựng dung dịch NaOH dư rồi đun nóng, thấy dung dịch từ phân lớp trở nên trong suốt
- Câu 109 : Phản ứng nào sau đây có phương trình ion rút gọn: H+ + OH‒ → H2O là?
A. Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
B. HCOOH + NaOH → HCOONa + H2O
C. HCl + NaOH → NaCl + H2O
D. 2NaOH + H2S → Na2S + 2H2O
- Câu 110 : Khi tiến hành sản xuất nhôm bằng phương pháp điện phân nóng chảy Al2O3 người ta tiến hành hòa tan oxit này trong criolit nóng chảy. Phát biểu nào sau đây không đúng với mục đích sử dụng criolit?
A. Criolit nóng chảy nổi lên trên tạo lớp màng bảo vệ nhôm nằm dưới
B. Tiết kiệm điện và tạo được chất lỏng dẫn điện tốt hơn
C. Cung cấp thêm ion nhôm cho sản xuất
D. Hạ nhiệt độ nóng chảy của oxit nhôm
- Câu 111 : Các dung dịch riêng biệt: Na2CO3, BaCl2, MgCl2, H2SO4, NaOH được đánh số ngẫu nhiên (1), (2), (3), (4), (5). Tiến hành một số thí nghiệm, kết quả được ghi lại trong bảng sau:
A. H2SO4, NaOH, MgCl2
B. H2SO4, MgCl2, BaCl2
C. Na2CO3, NaOH, BaCl2
D. Na2CO3, BaCl2, BaCl2
- Câu 112 : Dãy chuyển hóa nào sau đây có thể thực hiện được
A. KNO3 → HNO3 → AgNO3 → NO2 → Mg(NO3)2 → MgO
B. KNO3 → HNO3 → Cu(NO3)2 → NO2 → NaNO3 → NaNO2
C. KNO3 → NaNO3 → Ba(NO3)2 → NO2 → KNO3 → KNO2
D. KNO3 → Cu(NO3)2 → NO2 → NaNO3 → NaNO2
- Câu 113 : Cho 0,4 mol H3PO4 tác dụng hết với dung dịch chứa m gam NaOH, sau phản ứng thu được dung dịch X. Cô cạn X thu được 2,51m gam chất rắn. X có chứa
A. Na3PO4, NaOH
B. NaH2PO4, Na3PO4
C. Na2HPO4, Na3PO4
D. NaH2PO4, Na2HPO4
- Câu 114 : Cho 33,8 gam hỗn hợp X gồm hai muối M(HCO3)2 và RHCO3 vào dung dịch HCl dư thấy thoát ra 6,72 lít khí. Mặt khác, cho 33,8 gam hỗn hợp X trên vào 200 ml dung dịch Y gồm Ba(OH)2 0,5M và NaOH 1,5M, sau khi kết thúc các phản ứng thu được 2,24 lít khí, dung dịch Z và m gam kết tủa. Giá trị của m là
A. 19,7
B. 25,5
C. 39,4
D. 59,1
- Câu 115 : Điện phân (với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi) dung dịch chứa m gam muối M(NO3)n trong thời gian t, thấy khối lượng dung dịch giảm 43,616 gam và tại catot thoát ra kim loại M. Nếu điện phân với thời gian 1,5t, khối lượng dung dịch giảm 50,337 gam và tại catot thấy thoát ra 1,5792 lít khí (đktc). Tìm giá trị của m
A. 95,88 gam
B. 79,90 gam
C. 71,91 gam
D. 63,92 gam
- Câu 116 : Dung dịch của chất nào dưới đây có pH lớn nhất (các dung dịch cùng nồng độ mol) ?
A. K2SO4
B. NaHSO4
C. NaHCO3
D. KH2PO4
- Câu 117 : Thí nghiệm nào sau đây thu được dung dịch trong suốt và không có chất rắn ?
A. Cho Ba vào dung dịch H2SO4 dư
B. Cho Na vào dung dịch Ca(HCO3)2 dư
C. Cho CrO3 vào dung dịch NaOH loãng dư
D. Cho Cu vào dung dịch AgNO3 dư
- Câu 118 : Cho dãy các chất: Ag, Fe3O4, Al(OH)3, PbS, CaCO3 và Fe(NO3)2. Số chất trong dãy tác dụng với dung dịch H2SO4 loãng tạo khí là
A. 1
B. 2
C. 4
D. 3
- Câu 119 : Trộn V ml dung dịch H3PO4 0,08M với 250 ml dung dịch NaOH 0,32M dư thu được dung dịch X chứa 2 chất tan có cùng nồng độ mol. Giá trị của V là
A. 250 ml.
B. 400 ml
C. 2000 ml.
D.
- Câu 120 : Dung dịch X gồm NaOH xM và Ca(OH)2 yM. Dung dịch Y gồm NaOH yM và Ca(OH)2 xM.
A. 1,0
B. 2,0
C. 2,5
D. 1,5
- Câu 121 : Dung dịch nào sau đây không làm mất màu nước brom ?
A. Metyl fomat
B. Fructozơ
C. Anilin
D. Axit linoleic
- Câu 122 : Thực hiện thí nghiệm điều chế khí X, khí X được thu vào ống nghiệm theo hình vẽ sau:
A. Cho Cu vào dung dịch chứa NaHSO4 và Mg(NO3)2.
B. Cho Fe vào dung dịch H2SO4 đặc, nóng.
C. Cho bột CaCO3 vào dung dịch HCl loãng.
D. Cho Al vào dung dịch H2SO4 loãng.
- Câu 123 : Những nguồn năng lượng nào sau đây là nguồn năng lượng sạch không gây ô nhiễm môi trường?
A. Năng lượng hạt nhân, năng lượng mặt trời
B. Năng lượng than đá, năng lượng mặt trời, năng lượng hạt nhân
C. Năng lượng thuỷ lực, năng lượng gió, năng lượng mặt trời
D. Năng lượng than đá, dầu mỏ, năng lượng thuỷ lực
- Câu 124 : Tục ngữ có Câu 179Nước chảy đá mòn” trong đó về nghĩa đen phản ánh hiện tượng đá vôi bị hòa tan khi gặp nước chảy. Phản ứng hóa học nào sau đây có thể giải thích hiện tượng này?
A. CaCO3 + CO2 + H2O → Ca(HCO3)2
B. Ca(HCO3)2 → CaCO3 + CO2 + H2O
C. Ca(OH)2 + CO2 → CaCO3 + H2O
D. CaO + CO2 → CaCO3
- Câu 125 : Cho các phản ứng hóa học:
A. 1
B. 4
C. 3
D. 2
- Câu 126 : Cho các chất: AgNO3, Cu(NO3)2, MgCO3, Ba(HCO3)2, NH4HCO3, NH4NO3 và Fe(NO3)2. Nếu nung các chất trên đến khối lượng không đổi trong các bình kín không có không khí, rồi cho nước vào các bình, số bình có thể tạo lại chất ban đầu sau các thí nghiệm là
A. 5
B. 3
C. 6
D. 4
- Câu 127 : Hoà tan hoàn toàn một lượng Ba vào dung dịch chứa a mol HCl thu được dung dịch X và a mol H2. Trong các chất sau: Na2SO4, Na2CO3, Al, Al2O3, AlCl3, Mg, NaOH, NaHCO3. Số chất tác dụng được với dung dịch X là
A. 6
B. 5
C. 7
D. 4
- Câu 128 : Dung dịch X có chứa m gam chất tan gồm Na2CO3 và NaHCO3. Nhỏ từ từ đến hết 100ml dung dịch gồm HCl 0,4M và H2SO4 0,3M vào dung dịch X, sau khi phản ứng hoàn toàn thu được 0,04 mol CO2 và dung dịch Y. Nhỏ tiếp Ba(OH)2 dư vào dung dịch Y thu được 18,81 gam kết tủa. Giá trị m là
A. 9,72
B. 13,08
C. 11,40
D. 9,28
- Câu 129 : Điện phân (với điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi) với dung dịch X chứa a mol MSO4 (M là kim loại) và 0,3 mol KCl trong thời gian t giây, thu được 2,24 lít khí ở anot (đktc) và dung dịch Y có khối lượng giảm m gam so với khối lượng dung dịch X. Nếu thời gian điện phân là 2t giây thì thu được dung dịch Z có khối lượng giảm 19,6 gam so với khối lượng dung dịch X. Biết hiệu suất điện phân là 100%, các khí sinh ra không tan trong dung dịch. Có các phát biểu sau:
A. 3
B. 4
C. 2
D. 1
- Câu 130 : Dung dịch X chứa x mol NaOH và y mol Na2ZnO2; dung dịch Y chứa z mol Ba(OH)2 và t mol Ba(AlO2)2 (trong đó x < 2z). Tiến hành 2 thí nghiệm sau:
A. 0,075 và 0,10.
B. 0,15 và 0,05.
C. 0,075 và 0,05.
D. 0,15 và 0,10.
- Câu 131 : Hòa tan hoàn toàn 8,66 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 bằng dung dịch chứa hỗn hợp gồm 0,52 mol HCl và 0,04 mol HNO3 (vừa đủ), thu được dung dịch Y và 1,12 lít (đktc) hỗn hợp khí Z gồm NO và H2 có tỉ khối hơi đối với H2 là 10,8. Cho dung dịch Y tác dụng với một lượng vừa đủ dung dịch AgNO3 thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa nung đến đến khối lượng không đổi thu được 10,4 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây ?
A. 75
B. 79
C. 73
D. 77.
- Câu 132 : Thí nghiệm nào sau đây không tạo ra khí gây ô nhiễm ?
A. Cho Fe vào dung dịch H2SO4 đặc nóng.
B. Thêm từ từ dung dịch HCl và dung dịch NaHCO3.
C. Cho Cu vào dung dịch chứa Fe(NO3)3 và HCl.
D. Cho Zn vào dung dịch H2SO4 loãng.
- Câu 133 : Trong các phản ứng sau, có bao nhiêu phản ứng sinh ra đơn chất:
A. 6
B. 7
C. 5
D. 4
- Câu 134 : Cho vào ống nghiệm một vài tinh thể K2Cr2O7 , sau đó thêm tiếp khoảng 1ml nước và lắc đều để K2Cr2O7 tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu sắc của dung dịch X và Y lần lượt là:
A. màu vàng chanh và màu da cam
B. màu vàng chanh và màu nâu đỏ
C. màu nâu đỏ và màu vàng chanh
D. màu da cam và màu vàng chanh
- Câu 135 : Cho các hỗn hợp rắn dạng bột có tỉ lệ số mol trong ngoặc theo thứ tự chất như sau :
A. 6
B. 5
C. 4
D. 3
- Câu 136 : Cho hỗn hợp X gồm 0,05 mol CaCl2; 0,03 mol KHCO3; 0,05 mol NaHCO3; 0,04 mol Na2O; 0,03 mol Ba(NO3)2 vào 437,85 gam nước. Sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa Y và m gam dung dịch Z. Giá trị của m là
A. 440
B. 450
C. 420
D. 400
- Câu 137 : Cho sơ đồ phản ứng sau: NaOH → X1 → X2 → X3 → NaOH. Vậy X1, X2, X3 lần lượt là:
A. NaCl, Na2CO3 và Na2SO4.
B. Na2SO4, NaCl và NaNO3.
C. Na2CO3, NaHCO3 và NaCl.
D. Na2SO4, Na2CO3 và NaCl.
- Câu 138 : Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z và T:
A. MgCl2, CrCl3, AlCl3, KCl
B. CrCl3, AlCl3, MgCl2, KCl
C. CrCl3, MgCl2, KCl, AlCl3
D. AlCl3, CrCl3, MgCl2, KCl
- Câu 139 : Khí sinh ra trong trường hợp nào sau đây không gây ô nhiễm không khí?
A. Sản xuất nhôm từ quặng boxit.
B. Sản xuất rượu vang từ quả nho chín.
C. Sản xuất giấm ăn từ ancol etylic.
D. Sản xuất xút từ muối ăn
- Câu 140 : Thực hiện thí nghiệm như hình vẽ bên dưới:
A. Thí nghiệm trên mô tả cho quá trình ăn mòn điện hóa học.
B. Thanh Zn bị tan dần và khí hiđro thoát ra ở cả thanh Zn và thanh Cu.
C. Thanh Zn bị tan dần và khí hiđro chỉ thoát ra ở phía thanh Zn.
D. Thanh Zn là cực âm và thanh Cu là cực dương của pin điện.
- Câu 141 : Cho dãy các chất: NaOH, Sn(OH)2, Pb(OH)2, Al(OH)3, Cr(OH)3. Số chất trong dãy có tính chất lưỡng tính là
A. 1
B. 3
C. 4
D. 2
- Câu 142 : Cho V ml dung dịch K2Cr2O7 0,1M vào dung dịch HC1 đặc, dư thu được 1,344 lít khí Cl2 (đktc). Giá trị của V là
A. 100
B. 300
C. 400
D. 200
- Câu 143 : Hòa tan hết 8,1 gam kim loại M vào dung dịch HCl lấy dư thấy thu được 10,08 lít khí H2 (đktc). Nhận xét về kim loại M là đúng?
A. M tác dụng với dung dịch HCl và NaOH.
B. M là kim loại nặng.
C. M có độ dẫn điện lớn hơn so với Cu.
D. M được điều chế bằng nhiệt luyện
- Câu 144 : Cho các phát biểu sau:(a) Thép là hợp kim của sắt chứa từ 2–5% khối lượng cacbon.
A. 3
B. 2
C. 4
D. 5
- Câu 145 : Nung m gam hỗn hợp X gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi, thu được chất rắn Y. Cho Y vào nước dư, thu được 0,25m gam chất rắn Z và dung dịch E. Nhỏ từ từ dung dịch HCl 1M vào E, khi khí bắt đầu thoát ra cần dùng V1 lít dung dịch HCl và khi khí thoát ra hết, thì thể tích dung dịch HCl đã dùng là V2 lít. Tỉ lệ V1 : V2 là:
A. 2 : 3
B. 3 : 5
C. 5 : 6
D. 3 : 4
- Câu 146 : Một loại phân kali chứa 59,6% KCl, 34,5% K2CO3 về khối lượng, còn lại là SiO2. Độ dinh dưỡng của loại phân bón trên là
A. 61,10
B. 60,20
C. 50,70
D. 49,35
- Câu 147 : Hãy cho biết dùng quỳ tím có thể phân biệt được dãy các dung dịch nào sau đây?
A. glyxin, lysin, axit glutamic
B. glyxin, valin, axit glutamic
C. alanin, axit glutamic, valin
D. glyxin, alanin, lysin
- Câu 148 : Tiến hành các thí nhiệm:
A. 1
B. 4
C. 2
D. 3
- Câu 149 : Dung dịch NaOH loãng tác dụng được với tất cả các chất thuộc dãy nào sau đây?
A. CO, H2S, Cl2, dung dịch AlCl3, C6H5OH.
B. Al2O3, CO2, dung dịch NaHCO3, dung dịch ZnCl2, NO2.
C. Dung dịch NaAlO2, Zn, S, dung dịch NaHSO4.
D. NO, dung dịch Cu(NO3)2, dung dịch NH4Cl, dung dịch HCl.
- Câu 150 : Hấp thụ hoàn toàn V lít CO2 vào 250ml dung dịch hỗn hợp NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí. Cho Y tác dụng với Ba(OH)2 dư thấy xuất hiện 34,05 gam kết tủa trắng. Biết các khí đo ở đktc, giá trị của a là
A. 0,5M.
B. 0,7M.
C. 0,6M.
D. 0,9M.
- - Trắc nghiệm Hóa học 12 Bài 2 Lipit
- - Trắc nghiệm Hóa học 12 Bài 3 Khái niệm về Xà phòng và Chất giặt rửa tổng hợp
- - Trắc nghiệm Hóa học 12 Bài 4 Luyện tập Este và Chất béo
- - Trắc nghiệm Hóa học 12 Bài 5 Glucozơ
- - Trắc nghiệm Hóa học 12 Bài 6 Saccarozơ, Tinh bột và Xenlulozơ
- - Trắc nghiệm Hóa học 12 Bài 7 Luyện tập Cấu tạo và tính chất của Cacbohidrat
- - Trắc nghiệm Hóa học 12 Bài 9 Amin
- - Trắc nghiệm Hóa học 12 Bài 10 Amino axit
- - Trắc nghiệm Hóa học 12 Bài 11 Peptit và Protein
- - Hóa học 12 Bài 12 Luyện tập Cấu tạo và tính chất của Amin, Amino axit và Protein

