Đề thi thử THPT Quốc Gia - ĐH môn hóa năm 2015, Đề...
- Câu 1 : Cho phản ứng sau: KMnO4 + HOOC-COOH + H2SO4
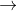 CO2 + MnSO4 + H2SO4 + H2O
CO2 + MnSO4 + H2SO4 + H2O A 30
B 31
C 32
D 33
- Câu 2 : Cho hình vẽ về cách thu khí trong phòng thí nghiệm
A H2, N2, O2, CO2, HCl, H2S
B O2, N2, H2, CO2.
C NH3, HCl, CO2, SO2, Cl2
D NH3, O2, N2, HCl, CO2
- Câu 3 : Chỉ từ các chất: Zn,S, dung dịch FeSO4 và dung dịch H2SO4 loãng (điều kiện có đủ), có bao nhiêu phương pháp điều chế khí H2S (mỗi phương pháp không dùng quá 2 phản ứng hóa học)?
A 3
B 4
C 2
D 5
- Câu 4 : Trong các loại phân bón : NH4Cl, (NH2)2CO ,(NH4)2SO4 ,NH4NO3 .Phân nào có hàm lượng đạm cao nhất :
A (NH2)2CO
B (NH4)2SO4
C NH4Cl
D NH4NO3
- Câu 5 : Hiện tượng hình thành thạch nhũ trong hang động và xâm thực của nước mưa vào đá được giải thích bằng PTHH nào dưới đây?
A CaO + H2O → Ca(OH)2
B CaCO3 + CO2 + H2O
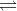 Ca(HCO3)2
Ca(HCO3)2C Ca(OH)2 + 2CO2 → Ca(HCO3)2
D CaCO3 + 3CO2 + Ca(OH)2 + H2O → 2Ca(HCO3)2
- Câu 6 : Cho 25,24 gam hỗn hợp X chứa Al, Zn, Mg, Fe phản ứng vừa đủ với 787,5 gam dung dịch HNO3 20% thu được dung dịch chứa m gam muối và 0,2 mol hỗn hợp khí Y (gồm N2O và N2) có tỉ khối so với H2 là 18. Giá trị của m là
A 163,60.
B 153,13.
C 184,12.
D 154,12.
- Câu 7 : Xét cân bằng: N2O4 (k) ⇄ 2NO2 (k) ở 250C. Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2
A tăng 9 lần.
B tăng 3 lần.
C tăng 4,5 lần.
D giảm 3 lần.
- Câu 8 : Nguyên tử của nguyên tố X có electron ở mức năng lượng cao nhất là 3p. Nguyên tử của nguyên tố Y cũng có electron ở mức năng lượng 3p và có một electron ở lớp ngoài cùng. Nguyên tử X và Y có số electron hơn kém nhau là 2. Nguyên tố X, Y lần lượt là:
A kim loại và kim loại.
B phi kim và kim loại.
C kim loại và khí hiếm.
D khí hiếm và kim loại.
- Câu 9 : Cho hỗn hợp bột X chứa a mol Cu và b mol Fe vào dung dịch chứa c mol AgNO3 thu được chất rắn Y không phản ứng với dung dịch HCl nhưng có phản ứng với dung dịch FeCl3. Mối quan hệ giữa a, b, c là
A 2a ≤ c < 2a + 2b.
B 2b < c ≤ 2a + b.
C 2a ≤ c ≤ 2a + 2b.
D 2b ≤ c < 2a + 2b.
- Câu 10 : Hoà tan 13,68 gam muối MSO4 vào nước được dung dịch X. Điện phân X (với điện cực trơ, cường độ dòng điện không đổi) trong thời gian t giây, được y gam kim loại M duy nhất ở catot và 0,035 mol khí ở anot. Còn nếu thời gian điện phân là 2t giây thì tổng số mol khí thu được ở cả hai điện cực là 0,1245 mol. Giá trị của y là
A 4,788
B 4,480
C 1,680
D 3,920
- Câu 11 : Cho lần lượt các chất sau : MgO, NaI, FeS, Fe3O4, Fe2O3, FeO, Fe(OH)2, Fe(OH)3, FeSO4, Fe2(SO4)3 tác dụng với dung dịch H2SO4 đặc, nóng. Số phản ứng oxi hoá - khử là :
A 9
B 8
C 7
D 6
- Câu 12 : Chất nào sau đây làm khô khí NH3
A P2O5
B H2SO4 đ
C CuO bột
D NaOH rắn
- Câu 13 : Số chất hoặc dung dịch có pH > 7 là:
A 7
B 3
C 1
D 5
- Câu 14 : Hòa tan hoàn toàn m gam Al2(SO4)3 vào nước được dung dịch X. Nếu cho 500ml dung dịch NaOH 2M vào X thì thu được 2a gam kết tủa.Mặt khác nếu cho 550 ml dung dịch NaOH 2M vào X thì thu được a gam kết tủa. Giá trị của m là
A 51,3 gam.
B 59,85 gam.
C 34,2 gam.
D 58,4 gam.
- Câu 15 : Cho 200 ml dung dịch Ba(OH)2 0,1M vào 300 ml dung dịch NaHCO3 0,1M, thu được dung dịch X và kết tủa Y. Cho từ từ dung dịch HCl 0,25M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Biêt các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
A 80
B 160
C 60
D 40
- Câu 16 : Dãy kim loại bị thụ động trong axit HNO3 đặc, nguội là
A Fe, Al, Cr
B Fe, Al, Ag
C Fe, Al, Cu
D Fe, Zn, Cr
- Câu 17 : Phản ứng tạo xỉ trong lò cao là
A CaCO3
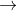 CaO + CO2.
CaO + CO2.B CaO + SiO2
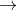 CaSiO3.
CaSiO3.C CaO + CO2
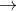 CaCO3.
CaCO3.D CaSiO3
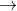 CaO + SiO2.
CaO + SiO2. - Câu 18 : Có phương trình như sau: Arắn + H2SO4 đặc, nóng
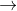 B + C. Biết B là axit. Dãy chất nào thỏa mãn
B + C. Biết B là axit. Dãy chất nào thỏa mãn A NaCl, NaNO3, Na2SO3
B NaCl, NaF, NaNO3
C Na2S, NaNO3, Na2SO3
D NaCl, Na2SO3, Na2HPO3
- Câu 19 : Đốt cháy hỗn hợp kim loại gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, sau phản ứng xảy ra hoàn toàn thu được 56,69 gam kết tủa. Phần trăm thể tích khí clo trong hỗn hợp X là
A 56,36%.
B 58,68%.
C 36,84%.
D 53,85%
- Câu 20 : Cho m gam bột Cu vào 400 ml dung dịch AgNO3 0,2M, sau một thời gian phản ứng thu được 7,76 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 5,85 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 10,53 gam chất rắn Z. Giá trị của m là
A 5,12
B 3,84
C 5,76
D 6,40
- Câu 21 : Màu trắng của những bức tranh cổ thường được vẽ bằng một loại bột trắng có thành phần PbCO3.Pb(OH)2, lâu ngày bị xám đen trong không khí. Có thể phục hồi lại màu trắng của những bức tranh này bằng hoá chất
A H2O2;
B O3
C Nước cường toan
D Nước Gia-ven
- Câu 22 : Cho các phản ứng sau :
A 4
B 5
C 6
D 3
- Câu 23 : Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 (M là kim loại có hóa trị khong đổi) trong 100 gam dung dịch H2SO4 39,2% thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chât tan duy nhất có nồng độ 39,41%. Kim loại M là
A Zn
B Cu
C Mg
D Ca
- Câu 24 : Cho hỗn hợp X gồm 2 kim loại kiềm tan hết trong 200ml dung dịch chứa BaCl2 0,3M và Ba(HCO3)2 0,8M thu được 2,8 lít H2 (ở dktc) và m gam kết tủa. Giá trị của m là
A 43,34
B 49,25
C 31,52
D 39,4
- Câu 25 : Người ta đã sản xuất khí metan thay thế một phần cho nguồn nguyên liệu hoá thạch bằng cách nào sau đây ?
A Thu khí metan từ khí bùn ao.
B Lên men các chất thải hữu cơ như phân gia súc trong lò biogaz.
C Lên men ngũ cốc.
D Cho hơi nước đi qua than nóng đỏ trong lò.
- Câu 26 : X là một chất hữu cơ được tạo bởi ba nguyên tố C, H và Cl. Qua sự phân tích định lượng cho thấy cứ 1 phần khối lượng H thì có 24 phần khối lượng C và 35,5 phần khối lượng Cl. Tỉ khối hơi của A so với hiđro bằng 90,75. Số đồng phân thơm của A là:
A 1
B 2
C 3
D 4
- Câu 27 : Cho 4,96 gam gồm CaC2 và Ca tác dụng hết với nước được 2,24 lít (đktc) hỗn hợp khí X. Dẫn X qua bột Ni nung nóng một thời gian được hỗn hợp Y. Cho Y qua bình đựng brom dư thấy thoát ra 0,896 lít ( đktc) hỗn hợp Z. Cho tỉ khối của Z so với hiđro là 4,5. Độ tăng khối lượng bình nước brom là:
A 0,4 gam.
B 0,8 gam.
C 1,2 gam.
D 0,86 gam.
- Câu 28 : Trong các tên gọi dưới đây, tên nào không phù hợp với chất : CH3CH(CH3)CH(NH2)COOH
A Axit 2-metyl-3-aminobutanoic.
B Valin.
C Axit 2-amino-3-metylbutanoic.
D Axit α-aminoisovaleric.
- Câu 29 : Độ linh động của nguyên tử H trong nhóm -OH của các hợp chất giảm dần theo thứ tự
A CH3COOH >C2H5OH > C6H5OH.
B CH3COOH > C6H5OH >C2H5OH.
C C2H5OH > C6H5OH > CH3COOH.
D C6H5OH > CH3COOH > C2H5OH.
- Câu 30 : Cho X, Y là hai chất thuộc dãy đồng đẳng của axit acrylic và MX < MY; Z là ancol có cùng số nguyên tử cacbon với X; T là este hai chức tạo bởi X, Y và Z. Đốt cháy hoàn toàn 11,16 gam hỗn hợp E gồm X, Y, Z, T cần vừa đủ 13,216 lít khí O2(đktc) , thu được khí CO2 và 9,36 gam nước. Mặt khác 11,16 gam E tác dụng tối đa với dung dịch chứa 0,04 mol Br2. Khối lượng muối thu được khi cho cùng lượng E trên tác dụng với KOH dư là :
A 5,44 gam
B 5,04 gam
C 5,80 gam
D 4,68 gam.
- Câu 31 : Cho các chất sau : CH3CH2CHO (1) ; CH2=CHCHO (2) ; CH≡CCHO (3) ; CH2=CHCH2OH (4) ; (CH3) 2CHOH (5). Những chất phản ứng hoàn toàn với lượng dư H2 (Ni, to) cùng tạo ra một sản phẩm là
A (2), (3), (4), (5).
B (1), (2), (4), (5).
C (1), (2), (3).
D (1), (2), (3), (4).
- Câu 32 : Cho bột Mg vào đietyl ete khan, khuấy mạnh, không thấy hiện tượng gì. Nhỏ từ từ vào đó etyl bromua, khuấy đều thì Mg tan dần thu được dung dịch đồng nhất. Các hiện tượng trên được giải thích như sau:
A Mg không tan trong đietyl ete mà tan trong etyl bromua.
B Mg không tan trong đietyl ete, Mg phản ứng với etyl bromua thành etyl magiebromua tan trong ete.
C Mg không tan trong đietyl ete nhưng tan trong hỗn hợp đietyl ete và etyl bromua.
D Mg không tan trong đietyl ete, Mg phản ứng với etyl bromua thành C2H5Mg tan trong ete.
- Câu 33 : Este có CTPT là C4H6O2, khi thuỷ phân trong môi trường axit thu được hỗn hợp các chất đều có khả năng tráng gương. CTCT thu gọn của este đó là
A HCOO-C(CH3) = CH2
B HCOO-CH=CH-CH3.
C CH3COO-CH=CH2.
D CH2 =CH-COO-CH3.
- Câu 34 : Phát biểu nào sau đây không đúng về xà phòng và chất tẩy rửa tổng hợp?
A Đều được sản xuất bằng cách đun nóng chất béo với dung dịch kiềm
B đều có khả năng hoạt động bề mặt cao, có tác dụng làm giảm sức căng bề nặt chất bẩn
C Xà phòng là hỗn hợp muối natri (kali) của axit béo, không nên dùng xà phòng trong nước cứng vì tạo ra muối kết tủa
D chất tẩy rửa tổng hợp không phải là muối natri của axit cacboxilic nên không bị kết tủa trong nước cứng
- Câu 35 : Cho sơ đồ chuyển hóa : CH3CH2Cl + KCN → X (1) ;
A CH3CH2NH2, CH3CH2COOH
B CH3CH2CN, CH3CH2CHO.
C CH3CH2CN, CH3CH2COOH.
D CH3CH2CN, CH3CH2COONH4.
- Câu 36 : Hỗn hợp X gồm Al, Fe3O4 và CuO, trong đó oxi chiếm 25% khối lượng hỗn hợp. Cho 1,344 lít khí CO (đktc) đi qua m gam X nung nóng, sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hòa tan hoàn toàn Y trong dung dịch HNO3 loãng (dư), thu được dung dịch chứa 3,08m gam muối và 0,896 lít khí NO (ở đktc, là sản phẩm khử duy nhất). Giá trị m gần giá trị nào nhất sau đây?
A 9,5
B 8,5
C 8,0
D 9,0
- Câu 37 : Poli(tetrafloetylen) hay thường gọi là teflon (CF2-CF2-)n được sản xuất từ clorofom qua các giai đoạn sau: 2n CHCl3
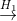 2nCHF2Cl
2nCHF2Cl 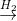 n CF2 = CF2
n CF2 = CF2 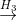 (-CF2 –CF2 -)n . Nếu xuất phát từ 17,505 tấn clorofom, với hiệu suất tương ứng của từng giai đoạn là: 79%; 81% và 80% thì lượng teflon thu được là:
(-CF2 –CF2 -)n . Nếu xuất phát từ 17,505 tấn clorofom, với hiệu suất tương ứng của từng giai đoạn là: 79%; 81% và 80% thì lượng teflon thu được là: A 3,7493 tấn.
B 4,6688 tấn.
C 7,342 tấn.
D 2,4995 tấn
- Câu 38 : Phương trình hóa học nào dưới đây là đúng?
A C6H5NH2 + HNO2
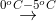 C6H5OH + N2 + H2O
C6H5OH + N2 + H2OB C6H5NH2 + HNO2 + HCl
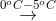 C6H5NH2+Cl- + 2H2O
C6H5NH2+Cl- + 2H2OC C2H5NH2 + HNO2 + HCl
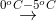 C2H5NH2+Cl- + 2H2O
C2H5NH2+Cl- + 2H2OD C2H5NH2 + HNO3
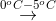 C2H5OH + N2O + H2O
C2H5OH + N2O + H2O - Câu 39 : Tripeptit X có công thức cấu tao sau: H2N-CH2-CONH-CH(CH3)-CONH-CH2COOH. Tên gọi của X là:
A Glyxylalaninglyxin
B Glyxylalanylglyxin
C Anlanylglyxylglyxyl
D Alanylglyxylalanin
- Câu 40 : Hỗn hợp M gồm một peptit X và một peptit Y (chúng cấu tạo từ 1 loại aminoaxit, tổng số nhóm –CO–NH– trong 2 phân tử là 5) với tỉ lệ số mol nX:nY=1:3. Khi thủy phân hoàn toàn m gam M thu được 81 gam glixin và 42,72 gam alanin. m có giá trị là :
A 110,28 gam
B 109,5 gam
C 104,28 gam
D 116,28 gam
- Câu 41 : Cho m gam một tripeptit X tạo thành từ amino axit no đơn chức mạch hở Y tác dụng với dung dịch NaOH dư (lượng NaOH gấp đôi lượng cần dùng), sau khí phản ứng kết thúc cô cạn dung dịch thu được m+26,64 gam chất rắn khan. Đốt m gam X cần 22,176 lít O2(đktc). Phân tử khối của X là :
A 203
B 259
C 245
D 217
- Câu 42 : Khi cho 2a mol một hợp chất hữu cơ X (chứa C, H, O) phản ứng hoàn toàn với Na sinh ra 2a mol khí, còn khi tác dụng với Na2CO3 dư thì sinh ra a mol khí. Chất X là
A etylen glicol.
B axit ađipic.
C ancol o-hiđroxibenzylic.
D axit 2-aminopropanoic
- Câu 43 : X là hỗn hợp gồm ancol A; axit cacboxylic B (A, B đều đơn chức no, mạch hở) và este C tạo bởi A, B. Chia một lượng X làm hai phần bằng nhau: + Đốt cháy hết phần 1 được 55,275 gam CO2 và 25,425 gam H2O. + Xà phòng hóa phần 2 bằng một lượng NaOH vừa đủ rồi cô cạn được ancol A và muối khan D. Đốt cháy hoàn toàn D được 15,9 gam Na2CO3 và 46,5 gam hỗn hợp CO2; H2O. Oxi hóa lượng ancol A thu được ở trên bằng lượng dư CuO; đun nóng được anđehit E. Cho E tác dụng với lượng dư dung dịch AgNO3 trong NH3 được 153,9 gam bạc. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng este C trong X là
A 33,33%
B 62,50%
C 72,75%
D 58,66%
- Câu 44 : Đốt cháy hoàn toàn 3,42 gam hỗn hợp gồm axit acrylic, vinyl axetat, metyl acrylat và axit oleic, rồi hấp thụ toàn bộ sản phẩm cháy vào dd Ca(OH)2 (dư). Sau phản ứng thu được 18 gam kết tủa và dd X. Khối lượng X so với khối lượng dd Ca(OH)2 ban đầu đã thay đổi như thế nào
A Tăng 2,70 gam.
B Giảm 7,74 gam.
C Tăng 7,92 gam.
D Giảm 7,38 gam.
- Câu 45 : Cho m gam hỗn hợp X gồm hai ancol đơn chức X1, X2 đồng đẳng kế tiếp (MX1 < MX2), phản ứng với CuO nung nóng, thu được 0,25 mol H2O và hỗn hợp Y gồm hai anđehit tương ứng và hai ancol dư. Đốt cháy hoàn toàn Y thu được 0,5 mol CO2 và 0,65 mol H2O. Mặt khác, cho toàn bộ lượng Y trên tác dụng với lượng dư dung dịch AgNO3 trong NH3 đun nóng, kết thúc các phản ứng thu được 0,9 mol Ag. Hiệu suất tạo anđehit của X1, X2 lần lượt là
A 50,00% và 66,67%.
B 33,33% và 50,00%.
C 66,67% và 33,33%.
D 66,67% và 50,00%.
- Câu 46 : Nguyên tử của một nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np5, trong hợp chất hidroxit tương ứng với oxit cao nhất % khối lượng R bằng 55,17%. R là:
A Cl
B Br
C S
D I
- Câu 47 : Cho phản ứng sau: KMnO4 + HOOC-COOH + H2SO4
CO2 + MnSO4 + H2SO4 + H2OTổng hệ số nguyên tối giản của phản ứng trên là:
A 30
B 31
C 32
D 33
- Câu 48 : Cho hình vẽ về cách thu khí trong phòng thí nghiệm
bằng cách dời nước. Hình vẽ bên có thể áp dụng để thu được những khí nào trong các khí sau đây ?
A H2, N2, O2, CO2, HCl, H2S
B O2, N2, H2, CO2.
C NH3, HCl, CO2, SO2, Cl2
D NH3, O2, N2, HCl, CO2
- Câu 49 : Số chất hoặc dung dịch có pH > 7 là:Nước Javen Nước Cl2 Dung dịch NaAlO2 Dung dịch Na2HPO3Dung dịch H2O2 Dung dịch K2S Dung dịch KClO Dung dịch KClO4
A 7
B 3
C 1
D 5
- Câu 50 : Có phương trình như sau: Arắn + H2SO4 đặc, nóng
B + C. Biết B là axit. Dãy chất nào thỏa mãn
A NaCl, NaNO3, Na2SO3
B NaCl, NaF, NaNO3
C Na2S, NaNO3, Na2SO3
D NaCl, Na2SO3, Na2HPO3
- Câu 51 : Cho các phản ứng sau :(a) H2S + SO2
(b) Na2S2O3 + dung dịch H2SO4 (loãng)
(c) SiO2 + Mg
(d) Al2O3 + dung dịch NaOH
(e) Ag + O3
(g) SiO2 + dung dịch HF
Số phản ứng tạo ra đơn chất là
A 4
B 5
C 6
D 3
- Câu 52 : Cho sơ đồ chuyển hóa : CH3CH2Cl + KCN → X (1) ; X + H3O+ (đun nóng) → Y (2)Công thức cấu tạo của X, Y lần lượt là
A CH3CH2NH2, CH3CH2COOH
B CH3CH2CN, CH3CH2CHO.
C CH3CH2CN, CH3CH2COOH.
D CH3CH2CN, CH3CH2COONH4.
- Câu 53 : Poli(tetrafloetylen) hay thường gọi là teflon (CF2-CF2-)n được sản xuất từ clorofom qua các giai đoạn sau: 2n CHCl3
2nCHF2Cl
n CF2 = CF2
(-CF2 –CF2 -)n . Nếu xuất phát từ 17,505 tấn clorofom, với hiệu suất tương ứng của từng giai đoạn là: 79%; 81% và 80% thì lượng teflon thu được là:
A 3,7493 tấn.
B 4,6688 tấn.
C 7,342 tấn.
D 2,4995 tấn
- - Trắc nghiệm Hóa học 12 Bài 2 Lipit
- - Trắc nghiệm Hóa học 12 Bài 3 Khái niệm về Xà phòng và Chất giặt rửa tổng hợp
- - Trắc nghiệm Hóa học 12 Bài 4 Luyện tập Este và Chất béo
- - Trắc nghiệm Hóa học 12 Bài 5 Glucozơ
- - Trắc nghiệm Hóa học 12 Bài 6 Saccarozơ, Tinh bột và Xenlulozơ
- - Trắc nghiệm Hóa học 12 Bài 7 Luyện tập Cấu tạo và tính chất của Cacbohidrat
- - Trắc nghiệm Hóa học 12 Bài 9 Amin
- - Trắc nghiệm Hóa học 12 Bài 10 Amino axit
- - Trắc nghiệm Hóa học 12 Bài 11 Peptit và Protein
- - Hóa học 12 Bài 12 Luyện tập Cấu tạo và tính chất của Amin, Amino axit và Protein

