nguyên tử - bảng tuần hoàn liên kết hóa học
- Câu 1 : X và Y là 2 nguyên tố thuộc cùng một chu kỳ, hai nhóm A liên tiếp. Số proton của nguyên tử Y nhiều hơn số proton của nguyên tử X. Tổng số hạt proton trong nguyên tử X và Y là 33. Nhận xét nào sau đây về X, Y là đúng?
A Độ âm điện của X lớn hơn độ âm điện của Y
B Đơn chất X là chất khí ở điều kiện thường.
C Lớp ngoài cùng của nguyên tử Y (ở trạng thái cơ bản) có 5 electron.
D Phân lớp ngoài cùng của nguyên tử X (ở trạng thái cơ bản) có 4 electron.
- Câu 2 : Nguyên tố Y là phi kim thuộc chu kì 3,có công thức oxit cao nhất là YO3. Nguyên tố Y tạo với kim loại M hợp chất có công thức MY, trong đó M chiếm 63,64% về khối lượng. Kim loại M là
A Zn
B Cu
C Mg
D Fe
- Câu 3 : Cho X (Z = 24), Y (Z = 26). X3+ , Y2+ có cấu hình electron lần lượt là:
A [Ne]3d4, [Ne]3d44s2
B [Ne]3d3, [Ne]3d6
C [Ar]3d3, [Ar]3d6
D [Ar]3d3, [Ar]3d5
- Câu 4 : Ion X3+ có cấu hình electron là 1s22s22p63s23p63d3 , công thức oxit cao nhất của X là
A X2O5
B XO2
C X2O3
D XO3
- Câu 5 : Cấu hình electron của ion Cu2+ và Cr3+ lần lượt là:
A [Ar]3d9 và [Ar]3d14s2
B [Ar]3d74s2 và [Ar]3d14s2
C [Ar]3d9 và [Ar]3d3
D [Ar]3d74s2 và [Ar]3d3
- Câu 6 : Nhận định nào sau đây đúng khi nói về 3 nguyên tử:
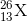 ,
,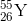 ,
, 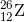 ?
? A X, Y thuộc cùng một nguyên tố hóa học
B X và Z có cùng tỉ khối
C X và Y có cùng số nơtron
D X, Z là 2 đồng vị của cùng một nguyên tố hóa học
- Câu 7 : Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân thì
A Độ âm điện tăng, bán kính nguyên tử giảm
B Tính kim loại giảm, bán kính nguyên tử tăng
C Tính phi kim tăng, độ âm điện giảm
D Tính kim loại tăng, tính phi kim giảm
- Câu 8 : Các nguyên tố X, Y, Z, T có số hiệu nguyên tử lần lượt là 14,15, 16, 17. Dãy gồm các phi kim xếp theo chiều giảm tính oxi hóa từ trái sang phải là
A T, Y, X, Z
B T, Z, Y, X
C Z, T, Y, X
D X, Y, Z, T
- Câu 9 : Một hợp chất MX có tổng số hạt (p, n, e) là 86 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 26 hạt. Số khối của X lớn hơn số khối của M là 12. Tổng số các hạt trong X nhiều hơn trong M là 18. Công thức phân tử của hợp chất MX là
A NaCl
B MgCl2
C K2S
D CaS
- Câu 10 : Tỉ số hạt mang điện và hạt không mang điện trong ion Fe3+ là
A 1,63
B 1,86
C 0,86
D 0,76
- Câu 11 : Các electron của anion X3- được phân bố trên 3 lớp , lớp thứ 3 có 8 electron. Số đơn vị điện tích hạt nhân nguyên tử của nguyên tố X là
A 15
B 18
C 21
D 16
- Câu 12 : Tổng số hạt cơ bản (p, n, e) trong phân tử MX3 là 196, trong đó số hạt mang điện tích nhiều hơn số hạt không mang điện là 60. Khối lượng nguyên tử của X lớn hơn của M là 8. Tổng số hạt (p, n ,e) trong X- nhiều hơn trong M3+ là 16. M và X lần lượt là
A Al và Br
B Cr và Cl
C Al và Cl
D Cr và Br
- Câu 13 : Nguyên tử của nguyên tố X có tổng số hạt (p,n,e) là 115 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Cấu hình electron nguyên tử của nguyên tố X là:
A 1s22s22p63s23p6
B 1s22s22p63s23p63d104s24p5
C 1s22s22p63s23p5
D 1s22s22p63s23p63d104s1
- Câu 14 : Đồng trong tự nhiên có 2 đồng vị là
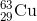 và
và 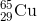 . Khối lượng nguyên tử trung bình của đồng là 63,54. Thành phần % theo khối lượng của
. Khối lượng nguyên tử trung bình của đồng là 63,54. Thành phần % theo khối lượng của 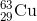 trong Cu2S là giá trị nào trong các giá trị sau (Cho S = 32) ?
trong Cu2S là giá trị nào trong các giá trị sau (Cho S = 32) ? A 39,94
B 29,15
C 58,31
D 21,69
- Câu 15 : Hợp chất X cấu tạo từ các ion của 2 nguyên tố A và B có dạng AB2. Trong phân tử X có số hạt mang điện của B nhiều hơn số hạt mang điện của A là 44 hạt, tổng số proton trong X là 46. Công thức phân tử của X là
A MgCl2
B CaCl2
C MgBr2
D CaBr2
- Câu 16 : Oxit cao nhất của một nguyên tố ứng với công thức R2O5 hợp chất của nó với hidro có %H = 8,82. Vị trí của R trong bảng tuần hoàn là
A Số thứ tự 7, chu kỳ 2, nhóm V A
B số thứ tự 15, chu kỳ 3, nhóm V A
C số thứ tự 13, chu kỳ 4, nhóm V A
D số thứ tự 23, chu kỳ 3, nhóm V B.
- Câu 17 : Tổng số hạt mang điện trong phân tử XY2 bằng 116. Số hạt mang điện trong hạt nhân nguyên tử X nhiều hơn số hạt mang điện trong hạt nhân nguyên tử Y là 20.
- Câu 18 : Các chất mà phân tử không phân cực là:
A HBr, CO2, CH4
B Cl2 , CO2 , C2H2
C NH3 , Br2 , C2H4
D HCl , C2H2 , Br2
- Câu 19 : Dãy gồm các phân tử có cùng bản chất liên kết là:
A NH3 , O2, SO2, NaOH
B HCl , CO2, H2SO4 , NH3
C NaCl, CaO, CH3COONa, CaS
D CH4, NaHCO3 , H2, HNO3
- Câu 20 : Dãy chất nào sau đây được sắp xếp theo chiều tăng dần sự phân cực liên kết trong phân tử?
A F2, K2S , H2S
B K2S , F2 , H2S
C F2, H2S , K2S
D K2S , H2S , F2
- Câu 21 : Cấu hình electron phân lớp ngoài cùng của nguyên tố A là 3s1 , còn nguyên tố B là 3s23p5. Vậy liên kết giữa A và B thuộc loại liên kết nào?
A Liên kết cộng hóa trị có cực
B Liên kết ion
C Liên kết cho – nhận
D Liên kết hidro
- Câu 22 : Số hiệu nguyên tử của nguyên tố X là 16, của nguyên tố Y là 1. Vậy hợp chất của X và Y có bản chất liên kết gì?
A Liên kết ion
B Liên kết cộng hóa trị có cực
C Liên kết cho – nhận
D Liên kết cộng hóa trị và liên kết cho – nhận
- Câu 23 : Những nhóm hợp chất nào dưới đây không tuân theo quy tắc bát tử?
A H2O, NH3 , PCl3 , Al2S3
B NO2 , PCl5 , BH3
C Al2O3 , PH3 , H2S , P2O5
D NH3, AlCl3 , SO2
- Câu 24 : Các nguyên tố X (Z= 8), Y (Z = 16), T (Z = 19) , G (Z = 20) có thể tạo được tối đa bao nhiêu hợp chất ion và hợp chất cộng hóa trị chỉ gồm hai nguyên tố?
A Ba hợp chất ion và ba hợp chất cộng hóa trị.
B Hai hợp chất ion và 4 hợp chất cộng hóa trị
C Năm hợp chất ion và một hợp chất cộng hóa trị
D Bốn hợp chất ion và hai hợp chất cộng hóa trị
- Câu 25 : Cho độ âm điện của các nguyên tố như sau: O (3,44), Cl(3,16) , Mg (1,31), C (2,55), H (2,2). Trong các phân tử: MgO, CO2, CH4, Cl2O. Số chất có kiểu liên kết cộng hóa trị có cực là
A 2
B 1
C 3
D 4
- Câu 26 : Nguyên tử của nguyên tố X có tổng số electron thuộc phân lớp p là 11. Điện tích hạt nhân nguyên tử của nguyên tố Y là +14,418.10-19 C (cu-lông). Liên kết giữa X và Y thuộc loại liên kết
A Kim loại
B cho – nhận
C cộng hóa trị có cực
D ion
- Câu 27 : (ĐHKB – 2012) : Phát biểu nào sau đây là sai?
A Nguyên tử kim loại thường có 1,2 hoặc 3 electron ở lớp ngoài cùng.
B Các nhóm A bao gồm các nguyên tố s và nguyên tố p.
C Trong một chu kì, bán kính nguyên tử kim loại nhỏ hơn bán kính nguyên tử phi kim.
D Các kim loại thường có ánh kim do các electron tự do phản xạ ánh sáng nhìn thấy được.
- Câu 28 : (ĐHKA – 2011) : Trong tự nhiên Clo có hai đồng vị bền:
chiếm 24,23% tổng số nguyên tử, còn lại là
. Thành phần % theo khối lượng của
trong HClO4 là:
A 8,92%
B 8,43%
C 8,56%
D 8,79%
- Câu 29 : (ĐHKA – 2010): Các nguyên tố từ Li đến F , theo chiều tăng của điện tích hạt nhân thì:
A bán kính nguyên tử và độ âm điện đều tăng
B bán kính nguyên tử tăng, độ âm điện giảm
C bán kính nguyên tử giảm, độ âm điện tăng
D bán kính nguyên tử và độ âm điện đều giảm
- Câu 30 : (ĐHKA – 2009): Cấu hình electron của ion X2+ là 1s22s22p63s23p63d6 . Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X thuộc:
A chu kỳ 4, nhóm VIII A
B chu kỳ 4, nhóm II A
C chu kỳ 3, nhóm VII B
D chu kỳ 4, nhóm VIII B
- Câu 31 : Nhận định nào sau đây đúng khi nói về 3 nguyên tử:
,
,
?
A X, Y thuộc cùng một nguyên tố hóa học
B X và Z có cùng tỉ khối
C X và Y có cùng số nơtron
D X, Z là 2 đồng vị của cùng một nguyên tố hóa học
- Câu 32 : Đồng trong tự nhiên có 2 đồng vị là
và
. Khối lượng nguyên tử trung bình của đồng là 63,54. Thành phần % theo khối lượng của
trong Cu2S là giá trị nào trong các giá trị sau (Cho S = 32) ?
A 39,94
B 29,15
C 58,31
D 21,69
- Câu 33 : Tổng số hạt mang điện trong phân tử XY2 bằng 116. Số hạt mang điện trong hạt nhân nguyên tử X nhiều hơn số hạt mang điện trong hạt nhân nguyên tử Y là 20.a, Xác định hai nguyên tố X, Y và vị trí của chúng trong bảng tuần hoàn.b, Viết cấu hình electron của các ion: X2+ , X3+ , Y2-c, Viết công thức cấu tạo của phân tử XY2.
- - Trắc nghiệm Hóa học 12 Bài 2 Lipit
- - Trắc nghiệm Hóa học 12 Bài 3 Khái niệm về Xà phòng và Chất giặt rửa tổng hợp
- - Trắc nghiệm Hóa học 12 Bài 4 Luyện tập Este và Chất béo
- - Trắc nghiệm Hóa học 12 Bài 5 Glucozơ
- - Trắc nghiệm Hóa học 12 Bài 6 Saccarozơ, Tinh bột và Xenlulozơ
- - Trắc nghiệm Hóa học 12 Bài 7 Luyện tập Cấu tạo và tính chất của Cacbohidrat
- - Trắc nghiệm Hóa học 12 Bài 9 Amin
- - Trắc nghiệm Hóa học 12 Bài 10 Amino axit
- - Trắc nghiệm Hóa học 12 Bài 11 Peptit và Protein
- - Hóa học 12 Bài 12 Luyện tập Cấu tạo và tính chất của Amin, Amino axit và Protein

