- Ôn tập về kim loại
- Câu 1 : Nhận xét nào sau đây không đúng ?
A Các kim loại kiềm đều mềm và nhẹ
B Các nguyên tư kim loại đều có cấu hình electron lớp ngoài cùng là ns1
C Các kim loại kiềm đều có tính khử mạnh
D Các kim loại kiềm đều có nhiệt độ nóng chảy rất cao
- Câu 2 : Trường hợp nào sau đây không xảy ra sự ăn mòn điện hoá?
A Sự ăn mòn vỏ tàu trong nước biển
B Sự gỉ của gang trong không khí ẩm
C Nhúng thanh Zn trong dung dịch H2SO4 có nhỏ vài giọt CuSO4
D Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ vài giọt dung dịch H2SO4
- Câu 3 : Có hỗn hợp gồm Si và Al. Hỗn hợp này phản ứng được với dãy các dung dịch nào sau đây:
A NaOH, KOH
B BaCl2 và AgNO3
C HCl, HF
D Na2CO3 và KHCO3
- Câu 4 : Hòa tan hết 2,24 g Fe trong 120ml dung dịch HCl 1M bị loãng được dung dịch X. Cho AgNO3 dư vào X tạo m g kết tủa. Giá trị của m là
A 19,40
B 17,22
C 21,54
D 18,30
- Câu 5 : Cho sơ đồ chuyển hóa trong dd Cr(OH)3
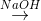 X
X 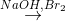 Y
Y A Na2CrO4 , CrBr3
B Na2CrO4 , Na2Cr2O7
C NaCrO2 , CrBr3
D NaCrO2 , Na2CrO4
- Câu 6 : Khi cho hỗn hợp Fe3O4 và Cu vào dung dịch H2SO4 loãng dư thu được chất rắn X và dung dịch Y. Dãy nào dưới đây gồm các chất đều tác dụng được với dd Y?
A BaCl2, HCl, Cl2.
B NaOH, Na2SO4,Cl2.
C KI, NH3, NH4Cl.
D Br2, NaNO3, KMnO4.
- Câu 7 : khi không có không khí , 2 kim loại nào đều tác dụng với HCl trong dung dịch tỉ lệ mol bằng nhau:
A Fe,Mg
B Fe,Al
C Na,Zn
D Na,Mg
- Câu 8 : Cho 4,2g bột Fe tác dụng với 250 ml dung dịch gồm AgNO3 0,2M và Cu(NO3)2 0,5M. Sau khi phản ứng hoàn toàn thu được m g chất rắn. Giá trị của m là:
A 10,00
B 5,9
C 9,1
D 8,6
- Câu 9 : Dẫn hơi nước đi qua bột sắt nung nóng theo sơ đồ hình vẽ
A Fe(OH)2
B Fe3O4
C Fe(OH)3
D Fe2O3
- Câu 10 : Hoà tan hoàn toàn m1 gam hỗn hợp 3 kim loại X,Y (đều có hoá trị II), Z ( hoá trị III) vào dung dịch HCl dư thấy có V lít khí thoát ra (ở đktc) và dung dịch X. Cô cạn dung dịch X thì được m2 gam muối khan. Biểu thức liên hệ giữa m1, m2, V là
A m2 = m1+ 35,5V
B m2 = m1+ 71V.
C 112m2 = 112m1 + 71V
D 112m2 = 112m1 + 355V.
- Câu 11 : Cho 13,36 gam hỗn hợp X gồm Cu và Fe3O4 vào dung dịch H2SO4 đặc nóng dư thu được V1 lít SO2 và dung dịch Y. Cho Y phản ứng với dung dịch NaOH dư thu được kết tủa T, nung kết tủa này đến khối lượng không đổi thu được 15,2 gam rắn Q. Nếu cũng cho lượng X như trên vào 400 ml dung dịch P chứa HNO3 và H2SO4 thấy có V2 lít khí NO là sản phẩm khử duy nhất thoát ra, còn 0,64 gam kim loại chưa tan hết. Các phản ứng xảy ra hoàn toàn, các khí đo ở đktc. Giá trị V1, V2 là
A 2,576 và 0,224
B 2,576 và 0,896
C 2,912 và 0,224
D 2,576 và 0,672
- Câu 12 : Hòa tan a gam tinh thể CuSO4.5H2O vào nước thu được dung dịch X. Điện phân dung dịch X với điện cực trơ và cường độ dòng điện là 1,93 (A). Nếu thời gian điện phân là t (s) thu được kim loại ở catod và 156,8 (ml) khí ở anod. Nếu thời gian điện phân là 2t (s) thì thu được 537,6 (ml) khí ở cả hai điện cực. Biết các khí đo ở đktc. Thời gian t và giá trị a lần lượt là
A 1400 s và 4,5 gam
B 1400 s và 7 gam
C 1400 s và 7 gam
D 700 s và 3,5 gam
- Câu 13 : Hoà tan hỗn hợp X gồm Cu và Fe2O3 trong 400 ml dung dịch HCl a mol/lít được dung dịch Y và còn lại 1 gam đồng không tan. Nhúng thanh Mg vào dung dịch Y, sau khi phản ứng xong, nhấc thanh Mg ra thấy khối lượng tăng 4 gam so với ban đầu và có 1,12 lít khí H2 (đktc) bay ra.(Giả thiết toàn bộ lượng kim loại thoát ra đều bám vào thanh Mg). Khối lượng của Cu trong X và giá trị của a là:
A 4,2g và a = 1M.
B 4,8g và 2M
C 1,0g và a = 1M
D 3,2g và 2M
- Câu 14 : Bốn kim loại K, Al, Fe và Ag được ấn định không theo thứ tự là X, Y, Z, và T. Biết rằng X và Y được điều chế bằng phương pháp điện phân nóng chảy; X đẩy được kim loại T ra khỏi dung dịch muối; và Z tác dụng được với dung dịch H2SO4 đặc nóng nhưng không tác dụng được với dung dịch H2SO4 đặc nguội. Các kim loại X, Y, Z, và T theo thứ tự là
A Al, K, Fe, và Ag.
B K, Fe, Al và Ag.
C K, Al, Fe và Ag.
D Al, K, Ag và Fe.
- Câu 15 : Cho hỗn hợp có a mol Zn tác dụng với dung dịch chứa b mol Cu(NO3)2 và c mol AgNO3. Kết thúc phản ứng hoàn toàn, thu được dung dịch X và chất rắn Y. Biết 0,5c < a < b + 0,5c. Kết luận nào sau đây đúng?
A X chứa 1 muối và Y có 2 kim loại.
B X chứa 2 muối và Y chứa 2 kim loại.
C X chứa 3 muối và Y chứa 2 kim loại.
D X chứa 2 muối và Y có 1 kim loại.
- Câu 16 : Có ba dung dịch riêng biệt: H2SO4 1M; KNO3 1M; HNO3 1M được đánh số ngẫu nhiên là (1), (2), (3).
A V2 = V1.
B V2 = 3V1.
C V2 = 2V1.
D 2V2 = V1.
- Câu 17 : Cho m gam hỗn hợp A gồm bột Fe và Cu có tỉ lệ khối lượng tương ứng là 2:3 vào 200ml dung dịch AgNO32M sau một thời gian phản ứng thu được 62,4 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X rồi thêm 27,3 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 28,7 gam chất rắn Z. Để hòa tan hết m gam hỗn hợp A bằng dung dịch HNO3 tạo sản phẩm khử duy nhất là NO thì cần số mol HNO3 tối thiểu là:
A 1,53
B 1,6
C 1,48
D 1,8
- Câu 18 : Cho 2,236 gam hỗn hợp A dạng bột gồm Fe và Fe3O4 hòa tan hoàn toàn trong 100ml dung dịch HNO3 có nồng độ C (mol/l), có 246,4 ml khí NO (dktc) thoát ra. Sau phản ứng còn lại 0,448 gam kim loại. Trị số của C là:
A 0,5M
B 0,68M
C 0,4M
D 0,72M
- Câu 19 : Tiến hành các thí nghiệm sau:- Ngâm một lá đồng trong dung dịch AgNO3.- Ngâm một lá kẽm trong dung dịch HCl loãng.- Ngâm một lá nhôm trong dung dịch NaOH.- Ngâm ngập một đinh sắt được quấn một đoạn dây đồng trong dung dịch NaCl.- Để một vật bằng gang ngoài không khí ẩm.- Ngâm một miếng đồng vào dung dịch Fe2(SO4)3.Số thí nghiệm xảy ra ăn mòn điện hóa là
A 4
B 2
C 3
D 1
- Câu 20 : Tiến hành các thí nghiệm sau:(a) Cho Mg vào dung dịch Fe2(SO4)3 dư;(b) Dẫn khí H2 (dư) qua bột MgO nung nóng;(c) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư;(d) Cho Na vào dung dịch MgSO4;(e) Nhiệt phân Hg(NO3)2;(g) Đốt Ag2S trong không khí;(h). Điện phân dung dịch Cu(NO3)2 với cực dương làm bằng đồng, cực âm làm bằng thép. Số thí nghiệm không tạo thành kim loại là
A 5
B 3
C 2
D 4
- Câu 21 : Cho sơ đồ chuyển hóa trong dd Cr(OH)3
X
Y(X ,Y là hợp chất của Crom). X,Y lần lượt là
A Na2CrO4 , CrBr3
B Na2CrO4 , Na2Cr2O7
C NaCrO2 , CrBr3
D NaCrO2 , Na2CrO4
- Câu 22 : Dẫn hơi nước đi qua bột sắt nung nóng theo sơ đồ hình vẽỞ nhiệt độ thấp hơn 570oC thì Fe bị nước oxi hóa thành
A Fe(OH)2
B Fe3O4
C Fe(OH)3
D Fe2O3
- Câu 23 : Có ba dung dịch riêng biệt: H2SO4 1M; KNO3 1M; HNO3 1M được đánh số ngẫu nhiên là (1), (2), (3).- Trộn 5 mL dung dịch (1) với 5 mL dung dịch (2), thêm bột Cu dư, thu được V1 lít khí NO.- Trộn 5 mL dung dịch (1) với 5 mL dung dịch (3), thêm bột Cu dư, thu được V2 lít khí NO.- Trộn 5 mL dung dịch (2) với 5 mL dung dịch (3), thêm bột Cu dư, thu được 3V1 lít khí NO.Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. So sánh nào sau đây đúng?
A V2 = V1.
B V2 = 3V1.
C V2 = 2V1.
D 2V2 = V1.
- Câu 24 : Tiến hành các thí nghiệm sau:(a) Cho Mg vào dung dịch Fe2(SO4)3 dư(b) Dẫn khí H2 dư qua MgO nung nóng(c) Cho dung dịch AgNO3 tác dụng với lượng dư Fe(NO3)2(d) Cho Na vào dung dịch MgSO4(e) Nhiệt phân Hg(NO3)2(g) Đốt Ag2S trong không khí(h) Điện phân dung dịch Cu(NO3)2 với cực dương làm bằng đồng và cực âm làm bằng thép.Số thí nghiệm không tạo thành kim loại là:
A 3
B 4
C 2
D 5
- - Trắc nghiệm Hóa học 12 Bài 2 Lipit
- - Trắc nghiệm Hóa học 12 Bài 3 Khái niệm về Xà phòng và Chất giặt rửa tổng hợp
- - Trắc nghiệm Hóa học 12 Bài 4 Luyện tập Este và Chất béo
- - Trắc nghiệm Hóa học 12 Bài 5 Glucozơ
- - Trắc nghiệm Hóa học 12 Bài 6 Saccarozơ, Tinh bột và Xenlulozơ
- - Trắc nghiệm Hóa học 12 Bài 7 Luyện tập Cấu tạo và tính chất của Cacbohidrat
- - Trắc nghiệm Hóa học 12 Bài 9 Amin
- - Trắc nghiệm Hóa học 12 Bài 10 Amino axit
- - Trắc nghiệm Hóa học 12 Bài 11 Peptit và Protein
- - Hóa học 12 Bài 12 Luyện tập Cấu tạo và tính chất của Amin, Amino axit và Protein

